烷基钯络合物是众多工业相关催化反应的重要中间体。而β-消除过程(β-氢消除和β-杂原子消除)是此类中间体的重要转化方式。近日,瑞士苏黎世联邦理工学院(ETH Zürich)Bill Morandi课题组系统研究了烷基钯配合物β-氢消除和β-杂原子消除竞争的影响因素。研究结果表明通过配体调控可以专一性实现任一消除过程,从而控制反应的选择性。此研究成果将为化学家们在设计催化反应时调控β-消除过程提供指导,以获得广泛的应用。相关成果发表在Nature Synthesis上。

(图片来源:Nature Synthesis)
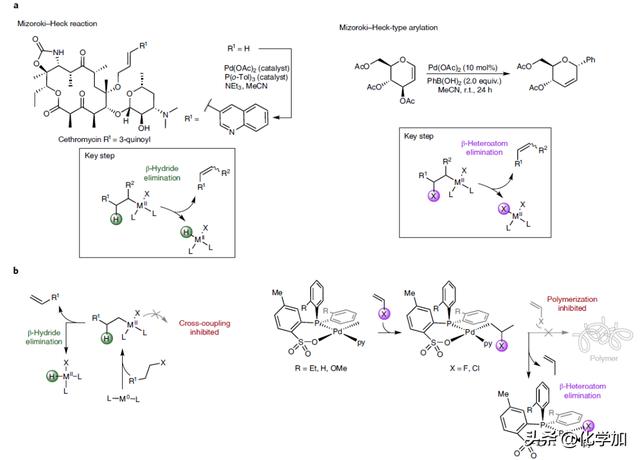
有机金属物种的发现和探索促使了合成方法的发展,对社会发展(包括重要药物的以及材料的制备等方面)产生了变革性的影响。一系列重要的催化反应,包括Ziegler-Natta聚合、Mizoroki-Heck交叉偶联和烷基C-H活化,均依赖于过渡金属-烷基中间体。这些中间体通常很不稳定,由于其很容易通过快速的β-消除(β-氢消除和β-杂原子消除)过程分别得到烯烃和M-H或M-X物种。因此,化学家们需要根据预期的合成产物结构,来阻止或促进这些消除过程。由于不同的反应过程会得到不同的产物,这使得在对催化反应的设计时需要对此类过程有更深的理解并做到精准预测。
β-氢消除过程是过渡金属-烷基络合物的主要转化途径,这经常阻碍其在交叉偶联反应中的应用(Fig. 1a)。β-杂原子消除与β-氢消除一样,普遍存在于过渡金属-烷基络合物的转化中,但对其研究和了解却较少。它是另一种过渡金属-烷基的转化途径,在聚合物化学中具有重要应用,其可以抑制乙烯和烯基卤或烯基醚及其衍生物的共聚过程(Fig. 1b)。目前已有许多化学计量β-X消除的例子被报道,其中涉及Ni, Pd, Co, Rh等金属。此外,这一过程也可应用于催化反应中,如Mizoroki-Heck型反应以及Paioti和Tran等课题组实现的不对称催化反应(Fig. 1c)。
由于两种β-消除反应均是通过金属-烷基络合物进行的,因此它们经常面临竞争,这会导致不同的烯烃产物的生成。因此对β-氢消除和β-杂原子消除竞争过程的深入研究将为控制这两类β-消除过程提供一定的指导作用,从而提高化学家们高化学选择性实现催化反应的能力。最近,瑞士苏黎世联邦理工学院(ETH Zürich)Bill Morandi课题组系统研究了烷基钯配合物中β-氢消除和β-杂原子消除竞争过程的影响因素,研究结果表明通过配体调控可以专一性实现任一消除过程,从而控制反应的选择性。此研究成果将为化学家们在设计催化反应时调控β-消除过程提供指导。

(图片来源:Nature Synthesis)
作者首先制备了几种具有合成相关X基团的底物,其中包括卤化物、磷酸酯、磺酸酯和羧酸酯等(Fig. 2a)。为了深入了解竞争过程中的动力学,作者使用1H NMR对反应过程进行监测。作者选用商业可得且高活性的Pd(PtBu3)2作为催化剂,其可以在室温下与底物快速发生氧化加成,随后经历β-氢消除和/或β-杂原子消除过程。作者根据观察到的pKaH与选择性之间呈S型相关,得出结论为好的离去基的存在会促进β-Χ消除过程(Fig. 2b)。此外,在β-氟消除和β-氢消除之间,β-氢消除过程具有较大的的优先性,这与模型预测的结果相一致(Fig. 2c)。接下来,作者选择最常用的Pd/PPh3体系,用同样的方式拟合函数仍观察到pKaH与选择性之间呈S型相关,这进一步证实了作者之前的结论(Fig. 2d)。实验数据表明,膦配体的选择会强烈影响β-杂原子消除过程的倾向性。有趣的是,尽管PPh3相对倾向于β-杂原子消除,但总体趋势是相似的,与离去基团X的pKaH仍然有明显的相关性。


(图片来源:Nature Synthesis)
为了深入了解强配体效应,作者对膦配体在反应中的作用进行了系统的研究。首先,通过对Pd(0)与对位不同电性基团取代的三芳基膦组成的催化体系进行尝试。通过将得到的选择性与配体的托尔曼电子参数(TEP)进行拟合,作者得出更富电子的配体有利于促进β-杂原子消除过程(Fig. 3a)。尽管P(p-NMe2-C6H4)3和PtBu3有着类似的托尔曼电子参数(2,054 VS 2,056 cm−1),但是其却产生相反的实验结果,这表明立体效应对反应有很大的影响(Fig. 3b)。由于PtBu3配体立体位阻较大,Pd(PtBu3)2在氧化加成后形成单膦T型Pd-芳基络合物需要较大的空间。相比之下,对空间要求较低的芳基膦Pd(0)络合物与芳基或苄基亲电试剂在发生氧化加成后会形成双膦平面方形Pd(II)络合物。作者认为这种在空间控制下反应中间体状态的变化可能是观察到差异的主要原因。随后作者通过Pd(PtBu3)2与过量的苄溴反应,通过31P{1H} NMR和XRD等测试手段证实了单膦Pd-芳基络合物的存在。接下来,作者通过原位变温核磁实验证实了反应过程中PtBu3是持续存在的,从而进一步支持了单膦中间体的存在。
为了进一步探索金属中间体β-氢消除和β-杂原子消除的选择性,作者又选择与PtBu3有类似的TEP的PCy3配体来探索其反应活性。实验结果表明当选用合适的底物(X = OMs)反应时,PtBu3体系得到β-氢消除和β-杂原子消除竞争的产物,而PCy3体系则专一性得到β-杂原子消除产物,这与作者所提出的金属络合物的配位状态相一致。此外,作者通过使用底物(X = OCOAr,Ar = p-NO2-C6H4)反应时,利用Pd(PtBu3)2催化专一性得到β-氢消除产物,而Pd(PCy3)2催化专一性得到β-杂原子消除产物,这进一步证实了作者提出的金属络合物的配位状态假设(Fig. 3c)。最后,通过实验作者得出β-氢消除和β-杂原子消除的选择性规则。使用富电子配体由于可以增加电子密度,并可以供给到C-X的σ*轨道,因此会促进β-杂原子消除。此外,小位阻配体可以促进双膦-Pd(II)中间体的形成,从而相对于β-氢消除来说更加有利于促进β-杂原子消除过程。相反,贫电子配体则会促进β-氢消除。而大位阻配体由于可以促进单膦-Pd(II)中间体的形成,会促进β-氢消除过程的发生(Fig. 3d)。


(图片来源:Nature Synthesis)
瑞士苏黎世联邦理工学院Bill Morandi课题组通过对单齿膦配体Pd络合物的计量反应研究,揭示了β-杂原子消除和β-氢消除竞争的控制因素。作者观察到β-杂原子消除过程取决于X基团的离去能力,通常来讲具有较低pKaH的X基团更容易发生β-杂原子消除。此外,富电子配体会促进β-杂原子消除,而贫电子配体会促进β-氢消除过程。总体来讲,电子效应的影响要远远小于空间位阻效应。配体的体积大小可以通过控制中间体的配位状态来影响反应。大位阻配体由于可以促进单膦-Pd(II)中间体的形成,而由于钯存在空的配位点可以强烈倾向于β-氢消除。而小位阻配体可以促进双膦-Pd(II)中间体的形成,从而促进β-杂原子消除。且当X基团的pKaH > 0时,可以在室温下选择性地实现β-氢消除。双膦-Pd(II)中间体途径通常倾向于使用小位阻配体,并在室温下优先消除pKaH < 6的X基团。此工作的发展将为化学家们在设计催化反应时调控β-消除过程提供指导,以获得广泛的应用。
,




