
1.(2020·浙江7月选考,1)水溶液呈酸性的是( )
A.NaCl B.NaHSO4
C.HCOONa D.NaHCO3
2.下列离子方程式不正确的是( )
A.热的纯碱溶液清洗油污:CO+H2OHCO+OH-
B.用铜电极电解硫酸铜溶液:2Cu2++2H2O2Cu↓+O2↑+4H+
C.用FeCl3饱和溶液制备Fe(OH)3胶体:
Fe3++3H2OFe(OH)3(胶体)+ 3H+
D.泡沫灭火器的灭火原理:Al3++3HCO===Al(OH)3↓+3CO2↑
3.(2021·重庆市云阳江口中学高三月考)下列应用与盐类水解无关的是( )
A.纯碱溶液可去除油污
B.用NaHCO3溶液和Al2(SO4)3溶液可以制作泡沫灭火剂
C.TiCl4溶于大量水加热制备TiO2
D.一定浓度NaHSO4溶液中加入甲基橙溶液呈红色
4.(2019·绍兴模拟)某兴趣小组为研究碳酸钠水解平衡与温度的关系,用数字试验系统测定一定浓度碳酸钠溶液的pH与温度的关系,得到曲线如图,下列分析不合理的是( )
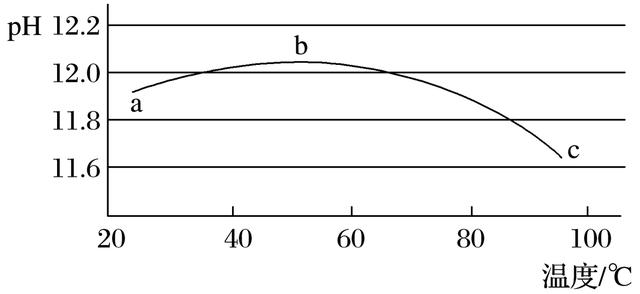
A.碳酸钠水解是吸热反应
B.ab段说明水解平衡向右移动
C.bc段说明水解平衡向左移动
D.水的电离平衡也对pH产生影响
5.(2020·湖南雅礼中学高三调研)下列物质用途或操作正确且与盐类水解有关的一组是( )
①用热饱和硫酸铵溶液清洗铁器表面的铁锈 ②明矾吸附水中杂质 ③用铁粉、氯化钠和炭粉的混合物作食品保鲜剂 ④在含氯化铁杂质的氯化铜溶液中加入过量的氧化铜,过滤除杂 ⑤在氯化氢气流中灼烧氯化镁晶体制备无水氯化镁 ⑥用硫酸铜和石灰乳配制波尔多液杀虫剂 ⑦用泡沫灭火器灭火 ⑧配制 Fe(NO3)2溶液时将Fe(NO3)2晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
A.①②④⑤⑦ B.③④⑥⑦⑧
C.①③④⑥⑦⑧ D.②③④⑤⑥⑦
6.(2020·贵阳月考)化学与社会、生活密切相关。下列对现象或事实的解释正确的是( )
|
选项 |
现象或事实 |
解释 |
|
A |
用热的烧碱溶液洗去油污 |
Na2CO3可直接与油污反应 |
|
B |
漂白粉在空气中久置变质 |
漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
|
C |
施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 |
K2CO3与NH4Cl反应生成氨会降低肥效 |
|
D |
FeCl3溶液可用于铜质印刷线路板制作 |
FeCl3能从含Cu2+的溶液中置换出铜 |
7.10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
|
温度 |
10 ℃ |
20 ℃ |
30 ℃ |
加热煮沸后冷却到50 ℃ |
|
pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为:该溶液pH升高的原因是HCO的水解程度增大,碱性增强。
(1)乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________(填“大于”或“小于”)NaHCO3的水解程度。
(2)丙同学认为:甲、乙的判断都不充分,还需要进一步补做实验来验证。
①只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙的判断正确。其中试剂X是______(填字母)。
A.Ba(OH)2溶液 B.BaCl2溶液
C.NaOH溶液 D.澄清石灰水
②将加热煮沸后的溶液冷却到10 ℃,若溶液的pH________(填“高于”“低于”或“等于”)8.3,则甲的判断正确。
③查阅资料,发现NaHCO3的分解温度为150 ℃,丙断言______(填“甲”或“乙”)的判断是错误的,理由是_________________________________________________________
________________________________________________________________________。
(3)关于NaHCO3饱和水溶液的表述正确的是________(填字母)。
a.c(Na+)=c(HCO)+c(CO)+c(H2CO3)
b.c(Na+)+c(H+)=c(HCO)+c(CO)+c(OH-)
c.HCO的电离程度大于HCO的水解程度
8.(2020·济南质检)请根据所学知识回答下列问题:
|
酸 |
电离常数 |
|
CH3COOH |
K=1.8×10-5 |
|
H2CO3 |
K1=4.3×10-7,K2=5.6×10-11 |
|
H2SO3 |
K1=1.54×10-2,K2=1.02×10-7 |
(1)NaHSO3溶液中共存在7种微粒,它们是Na+、HSO、H+、SO、H2O、__________、__________(填微粒符号)。
(2)常温下,物质的量浓度相同的下列溶液:
①NH4Cl ②NH4HCO3 ③(NH4)2SO4 ④NH4HSO4
溶液中c(NH)最大的是________,最小的是________(填序号)。
(3)常温下,物质的量浓度均为0.1 mol·L-1的六种溶液①NaOH、②NaCl、③Na2CO3、④H2SO3、⑤CH3COONa、⑥H2SO4,pH从大到小的排列顺序为___________________________(填序号)。
(4)常温时,AlCl3的水溶液呈酸性,原因是(用离子方程式表示)__________________________。把AlCl3溶液蒸干,灼烧,最后得到的固体产物主要是________________(填化学式)。
,




