第二单元 胶体的性质及其应用
一、 学习目标
1.了解分散系的概念;了解胶体的概念;了解胶体的性质;了解胶体的实际应用。
2.掌握胶体与溶液,悬浊液,乳浊液的区别;掌握胶体的精制方法;理解丁达尔效应,布朗运动和电泳现象产生的原因。
二.教学建议
1.充分利用初中已有的溶液、悬浊液、乳浊液的知识,列表比分散系的有关知识。要重视以旧带新,联系已学过的与胶体知识有关的基础,以达到边复习边旧知识、边学习新知识的目的。
2.结合实验和列表比较,从观察比较中认识胶体的本质特征。
3.胶体内容学习过程中学生会感到记忆难、应用难等问题,教学中要注意引导和帮助学生整理知识、归类知识。
第一节 胶体
一.学习目标
1.理解胶体的基本概念,了解胶体特征。
2.能够从分散质微粒的大小、分散系的性质等角度理解胶体与溶液、悬浊液、乳浊液的区别。
3.掌握胶体的本质特征,以及胶体的精制。理解氢氧化铁胶体的制法原理。
二、教学过程
1.我们平时所接触到的分散系一般有三种,即 ________、__________、_________,我们把分散系分成以上三种的依据是 _________,当分散质粒子直径小于1 nm时,是_________,大于100nm时,是_________,在1 nm~100nm之间时是 _________。
2.如何分离胶体与浊液_________,如何分离胶体与溶液_________;如何分离浊液与溶液_________,胶体净化的方法是_________,为什么可以采用该办法_____________。
3.胶体的形成不是物质_________的反映,而是物质的一种_______形式。根据分散剂的不同,可分为溶胶,如 _________;______溶胶,如_________溶胶,如_____等。
三、重点、难点点拨
1.如何理解胶体的本质特征和渗析的关系胶体粒子的直径在1 nm~100nm之间是胶体的本质特征,也是胶体区别于其他分散系的依据,同时也决定了胶体的性质。
胶体粒子直径较大,不能透过半透膜,但分子或离子可以透过半透膜,据此可以通过“渗析”的方法制某些胶体。渗析是一种分离操作,通过多次渗析或把半透膜袋放在流动的水中,可以使胶体得到更好的精制。
2.为什么有的高分子溶液具有胶体的某些性质?
高分子化合物溶于适当的溶剂中,就成为高分子溶液,它具有双重性,一方面由于分散质颗粒太小与溶胶粒子相近,表现出溶胶的某些特性,例如不能透过半透膜,因此高分子溶液可纳入胶体研究范畴。另一方面高分子溶液是分子分散体系,又具有某些真溶液的特点,与胶体有许多不同的地方。例如:高分子溶液一般不带电荷,溶胶粒子则带电荷。高分子溶液的稳定是它的高度溶剂化起了决定性作用,粒子不带电也能均匀地分散在溶液中。
高分子化合物能自动溶解于适当的溶剂中,当蒸发溶剂后,再加入溶剂仍然自动溶解。胶体溶液则不能由自动分散来获得,胶粒一旦凝聚出来,一般很难简单地用加人溶剂的方法使之复原。
3.胶体较稳定的原因:①胶体中胶粒体积小,被介质分子碰撞而不易上浮或下沉,凝析;②胶体中胶粒带有同性电荷,相互排斥的结果不易凝析出来。
4.胶粒带电的原因:胶体中单个胶粒的体积小,因而胶体中胶粒的表面积大,因而具备吸附能力。有的胶体中的胶粒吸附溶液中的阳离子而带正电;有的则吸附阴离子而带负电胶体的提纯,可采用渗析法来提纯胶体。使分子或离子通过半透膜从胶体里分离出去的操作方法叫渗析法。其原理是胶体粒子不能透过半透膜,而分子和离子可以透过半透膜。但胶体粒子可以透过滤纸,故不能用滤纸提纯胶体。
习题精析
[例1]下列关于胶体的说法中正确的是( )
(A)胶体外观不均匀 (B)胶粒做不停的,无秩序的运动
(C)胶粒不能通过滤纸 (D)胶体不稳定,静置后容易产生沉淀
[解析]胶粒可以透过空隙较大的滤纸,但不能透过空隙较小的半透膜。胶体是比较稳定的分散系。
[答案]B
[例2]胶体是比较稳定的分散系的主要原因是 A.胶粒直径在1 nm-100nm之间 B,同种胶体的粒子带有同种电荷 C.胶体溶液显电中性 D.胶粒是运动的
[解析]胶体稳定的原因是其中的胶粒带电荷,并且同种胶体的粒子带同种电荷,同种电荷相互排斥,因而胶体稳定。
[答案]B
[例3]下列各种物质中,常用渗析方法分离的是 ( )
(A)CaCO3和Na2CO3 (B)NaCl和KNO3
(C)CCl和水 (D)Fe(OH)3胶体和FeCl3溶液
[解析]渗析方法适用于胶体和溶液的分离。 [答案]D
[例4]下列两种物质混合后,所形成的分散系属于胶体的是( )
(A)溴水和汽油 (B)硫代硫酸钠和盐酸
(C)乙二醇和甘油 (D)鸡蛋清和甘油
[解析lA形成的是溴的有机溶液,B形成的是单质硫沉淀和NaCI溶液,C二者物质互溶,D形成的属高分子溶液,也属于胶体的范畴。
[答案]D
[例5]氯化铁溶液与氢氧化铁胶体具有的共同性质是( )。
(A)分散质颗粒直径都在l~100nm之间 (B)能透过半透膜
(C)加热蒸干、灼烧后都有氧化铁生成 (D)呈红褐色
[解析]从分散系角度来分类,氯化铁溶液和氢氧化铁胶体属于不同的分散系。氯化铁溶液属于溶液,其中的分散质微粒是Fe3 和Cl-离子。氢氧化铁胶体属于胶体,其中的分散质氢氧化铁构成的胶粒,分散质的直径要大一些。但两者加热蒸干、灼烧后,都会得到氧化铁。
[答案]C。

胶体针对性训练
(A组题)
1.制取Fe(OH)3胶体的离子方程式;下面正确的是( )
(A)Fe3 3H2O

(B)Fe3 3H2O

(C)Fe3 3H2O

(D)Fe3 3H2O

2.既能透过半透膜,又能透过滤纸的是( )
(A)NaCl溶液 (B)淀粉溶液 (C)酒精溶液 (D)Fe(OH)3胶体
3.用饱和的FeCl3溶液制取Fe(OH)3胶体,正确的操作是( )
(A)将FeCl3溶液滴人蒸馏水中
(B)将FeCl3溶液滴人热水中,生成棕黄色液体
(C)将FeCl3溶液滴人沸水中,并继续煮沸至生成红褐色液体
(D)将FeCl3溶液滴人沸水中,并继续煮沸至生成红褐色沉淀
4.将淀粉和KI的混合溶液装在羊皮纸制成的袋中,将此袋下半部浸泡在盛有蒸馏水的烧杯里,过一段时间后,取烧杯中液体进行实验。下列现象能证明半皮纸袋一定有破损的是( )
(A)加入碘水变蓝色 (B)加入NaI溶液不变蓝色
(C)加入AgN03溶液产生黄色沉淀 (D)加入溴水变蓝色
5.下列各组中,可用相同的方法除去混有的杂质的是( )
(A)淀粉溶液中混有少量NaCl;蔗糖中混有少量NaCl
(B)Fe(OH)3中混有少量盐酸;淀粉溶液中混有少量KI溶液
(C)Na2SiO3胶体中混合有少量NaHCO3;NaHC03中混有少量Na2CO3
(D)CO2中混有少量SO2;CO2中混有少量HCl
6.已知土壤胶粒带负电,因此在水稻田中,施用含氮量相同的下列化肥时,肥效最差的是( )
(A)硫铵 (B)碳铵 (C)硝铵 (D)氯化铵
7.下列属于胶体的是 ( )
①肥皂水 ②烟水晶 ③水玻璃 ④蔗糖 ⑤尿素 ⑥淀粉溶液
(A)只有⑥ (B)①②③ (C)①②⑥ (D)①②③④⑥
8.下列有关胶体的叙述正确的是 ( )
(A)胶体是均匀,透明的液体
(B)胶体粒子的大小决定了胶体丁达尔现象的产生
(C)胶体能透过半透膜,所以可用渗析法提纯
(D)制备胶体必须在加热条件下进行
9.当光束通过下列分散系时,能形成一条光亮通路的是 ( )
(A)食盐水 (B)碘酒 (C)淀粉溶液 (D)F(OH)3溶胶
10.分别将下列各组物质等体积混合,在室温下激烈振荡,静置后,能够形成均匀溶液的是 ( )
(A)四氯化碳、碘水 (B)甲醇、水 (C)汽油、水 (D)乙酸乙酯、水
11.在半透膜袋里盛有淀粉和溴化钠溶液,将半透膜悬挂在蒸馏水中。
(1)如何用实验证明淀粉未通过半透膜?
(2)要求只检验一种离子,就能证明钠离子、溴离子通过半透膜,写出检验该离子的实验方法?
(3)如何用实验证明两者已完全分离?
(4)如何证明半透膜破损?
(5)如何证明两者已部分分离?
(6)如何操作能使两者完全分离?
12.某一混合液中含有悬浮于混合液中的固体颗粒以及胶体和电解质NaCl,如何将它们分离出来?
(B组题)
1.有3g白色粉末,溶于10g热水中,冷却到室温时析出2g粉末,将析出的2g粉末再溶解于10g热水中,冷却到室温时析出1.5g。据此,可确定白色粉末是( )。
(A)纯净物 (B)混合物 (C)某种盐 (D)不能确定
2.纳米技术是正在崛起的新科技,它研究的粒子直径在1-100nm之间。在此范围内物质的性质发生很大变化。例如Cu的直径加工成几个纳米时,会在空气中剧烈燃烧。纳米TiO2,是理想的光催化剂,光照时在常温下可将汽车尾气中氮、硫的氧化物氧化成相应的酸,同时它可以将废水中的有害物质快速氧化成C02和H2O,此外它还可作抗菌材料等。以下有关说法中正确的是 ( )
(A)纳米铜比纳米铁金属活动性更强
(B)纳米铜在反应中可能作氧化剂
(C)纳米TiO2,在不向溶剂中均形成了胶体
(D)纳米TiO2有很强的氧化性
3.根据中央电视台报道,近年来,我国的一些沿江或沿海城市多次出现大雾天气致使高速公路关闭,航班停飞,雾属于下列分散系中的( )
(A)溶液 (B)悬浊液 (C)乳浊液 (D)胶体
4.用于渗析操作的半透膜的孔径是 ( )
(A)大于100nm (B)略小于1 nm
(C)介于1~100nm之间 (D)小于1 nm
5.下列关于胶体的叙述不正确的是( )
(A)有色玻璃是固溶胶
(B)胶体粒子是带电粒子,在溶液中自由移动
(C)胶体粒子通常不易聚集,因而胶体是比较稳定的分散系
(D)用渗析法可将胶体混合液里的K 、N03-等分离除去
6.溶液、胶体和浊液这三种分散系的根本区别( )
(A)是否是大量分子或离子的集合体 (B)分散质粒子直径的大小
(C)能否透过滤纸或半透膜 (D)是否均一、稳定、透明
7.不能发生丁达尔现象的分散系是( )
(A)碘酒 (B)无水酒精 (C)蛋白质溶液 (D)钴玻璃
8.有关胶体和溶液的区别,下列叙述中正确的是( )
(A)溶液呈电中性,胶体带电荷
(B)溶液中溶质粒子一定不带电,胶体中分散质粒子带有电荷
(C)通电后,溶液中溶质粒子分别向两极移动,胶体中分散质粒子向某一极移动
(D)溶液中通入一束光线没有特殊现象,胶体中通过一束光线出现明显的光带
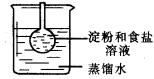
(A)细玻璃管内液面上升
(B)细玻璃管内液面不变
(C)蒸馏水遇碘酒变蓝
(D)蒸馏水遇AgNO3溶液有白色沉淀生成
10.下列分散系中,是胶体的是( )
①在1 mol·L-1的KI溶液中加入1 mol·L-1的AgNO3溶液,边加边振荡 ②将蔗糖加入水中③将花生油放入水中并振荡 ④蛋白质分散于水中 ⑤把1 mL水玻璃加入到10mLl mol·L-1的盐酸中,用力振荡 ⑥把1 mL饱和FeCl3溶液滴加入20mL沸水中,边滴边振荡
(A)①③④⑤ (B)①②④⑤ (C)④⑤⑥ (D)①④⑤⑥
11.分散质粒子的直径在___________nm~________nm之间的分散系叫做胶体,胶体按其分散剂的聚集状态不同可分为__________。区别胶体和溶液时通常用 __________,提纯胶体时,通常采用__________ 的方法。
12.分别设计化学实验,用最佳方法证明明矾溶于水时发生的下列变化
供选择的药品和仪器:明矾溶液,甲基橙试液,石蕊试液,酚酞试液,pH试纸,NaOH溶液,酒精灯,半透膜,聚光束仪
(1)证明明矾发生了水解反应
(2)证明其水解是一个吸热反应
(3)证明生成了胶体
第一节 胶体针对性训练题答案
(A组题)
1.B 2.AC 3.C 4.AD 5.BD 6.C 7;C 8.B 9.CD 10.B
11.(1)取烧杯内少量液体,向其中滴加碘水,发现不变蓝色。
(2)因Br-半径大于Na ,因此只要检验Br—即可说明;取烧杯中少量液体向其中滴加硝酸酸化的硝酸银溶液,生成浅黄色沉淀。
(3)经过多次更换烧杯中的水,最终取烧杯中少量液体,向其中滴加AsNO,,若无沉淀产生,则说明两者已完全分离。
(4)若用碘水检验出烧杯中的液体合淀粉,则说明半透膜破损。
(5)从半透膜袋中取出少量液体于试管中,滴加硝酸银溶液观察现象。若无淡黄色沉淀生成,说明液体中已不含溴化钠,淀粉跟溴化钠已完全分离。
(6)烧杯中的水要不断更换。
12.先将溶液过滤,将滤出的固体颗粒洗涤,干燥;再将滤液置于半透膜袋,悬挂在蒸馏水中,静置一段时间后,使电解质离子通过半透膜进入蒸馏水中,则袋中为胶体,从而分离。
(B组题)
1.B 2.D 3.D 4.B 5.D 6.B 7.A 8.D 9.AD 10.C
11.1 100 气溶胶 液溶胶和固溶胶 丁迭尔现象 渗析
12.(1)用pH试纸测明矾溶液 pH<7 证明溶液呈酸性
(2)加热溶液,用pH试纸测溶液pH,pH减小。
(3)用聚光束仪的光束照溶液,有丁达尔现象。
,