本月初(6月7日),2篇研究论文在《Cell》(即《细胞》杂志,刊登过许多重大的生命科学研究进展,与《自然》和《科学》并列为全世界最权威的学术杂志之一)同时发表,证实了“记忆能够被遗传”。
传统的生物学认为,生殖细胞中的遗传信息与躯体影响是分开的,并在很长的时间内被奉为生物学的基本法则之一。然而,上述两个研究发现,至少在线虫(C. elegans)这种模式生物中,记忆能够被遗传,并维持3代到4代。
这并不是科学家们第一次类似的发现。
2014年,美国亚特兰大艾文理大学精神病学部门由布莱恩‧迪亚斯博士(Dr. Brian Dias)带领团队,通过小鼠实验后发现,小鼠对特定事件的恐惧可导致类似抑郁症的行为,而这种恐惧和行为模式可遗传给下一代。(Katharina, Gapp;Ali, Jawaid;Peter, Sarkies;et al. Implication of sperm RNAs in transgenerational inheritance of the effects of early trauma in mice[J] . Nature Neuroscience, 2014,17(5):667-9.)
该恐惧反应的遗传是经由化学基因转换时改变了后代的神经系统,接下来的世代受到特定事物的刺激反应时,都会出现同样的恐惧和类似行为,哪怕这些后代此前从未经历过特定事件。
看到这里,可能读者会有所疑问,既然“记忆能够被遗传”,那么抑郁/双相障碍等常见的精神心理障碍是否也可遗传?这是否更加证实了大部分精神科医生所说的“遗传因素”?
我曾专门撰文分析双相障碍的遗传因素问题。时下主流精神病学界认为,双相情感障碍的病因遗传因素占80%。但我们通过追踪文献引用源,分析其数量遗传学的研究方法发现,这个说法站不住脚,更准确地表达应为:“双相情感障碍的遗传因素和共享环境因素总共比例为80%”。
而且,文章开头提及的3个实验中的“遗传”也并非大众所理解的、传统的遗传(特定致病基因或遗传物质的遗传),而是通过表观遗传学机制来进行的——基因本身并没有产生改变,改变的是基因的表达方式。
基因表达是什么意思?国内著名科普平台“果壳网”曾对此作出过生动的解释:
基因可以看成储存在细胞里的“生命图纸”,而基因表达就是把这些“图纸”变成“产品”的过程。基因表达的“产品”通常是各种蛋白质(也可以是RNA),我们在生物书上学到的DNA转录成RNA、RNA翻译成蛋白质就是基因表达的重要步骤。
“基因表达改变”和“基因本身改变”有着本质的不同。基因表达改变指的是细胞使用“图纸”的方式变了:它们可能是挑选了不同部分的“图纸”来制作“产品”,也可能使用图纸制作的“产品”数量增加或者减少了。“产品”的变化会影响细胞的生理功能,但在这个过程中,作为“图纸”的基因本身没有发生变化。
基因表达的改变非常常见,甚至是维持人体生理功能、机体适应外界环境所必需的“技能”。前不久有报道指出,熬夜也会导致基因表达发生改变。
心理压力、饮食、体育锻炼、成长环境、药物治疗及心理干预都可能引起基因表达的改变;而且,基因表达产生变化后,也可通过改变以上的因素令其再次变化。
基于以上发现,我们可以大胆设想:即使抑郁/双相障碍等常见精神心理障碍的发病受到表观遗传学机制的影响,也可以通过改变成长环境、药物治疗、心理干预等方式,令基因表达再次发生改变,减少或消除其对个体和后代的负面影响。
而且,对于那些遭受过叠加性心理创伤,存在病理性记忆的患者而言,其“记忆”本身也不是不可改变的。
科研已经证实,记忆存在再巩固的过程。已经巩固的记忆被提取激活后,可进入不稳定的状态,可持续6小时,在此时间窗内,通过药物或行为干预的方式可以将原始记忆增强、减弱或改变。(《人类记忆再巩固研究现状及临床应用》,李永芬等,2017)
我们据此推测,我们创立的深度催眠下的创伤修复技术(TPTIH)正是在深度催眠下激活了相关创伤记忆,令其处于不稳定状态,在6小时时间窗内,对此进行快速修复处理,新的记忆得以快速巩固。
而且,患者康复后并拥有积极、乐观、坚韧的良好性格后,同样也能通过表观遗传学遗传给下一代。
从这个角度来看,“双相障碍是否可遗传”这个问题在临床中已不重要了,医生不应过多地向患者、家属传递“遗传因素”的信息,以免引起误解和恐惧;更不应误以为既然有遗传因素就一定无法改变。
随着人类对脑科学和心理的研究越来越深入,医生、患者及家属,应理性、客观对待精神心理障碍的病因尤其是所谓的遗传因素,免于恐惧,摆正心态,积极地寻求治疗方法,化弊为利。
——何日辉
(下文来源公众号:iNature)
许多人推测大脑活动可能以某种方式产生可遗传的变化,这将影响下一代的命运。然而,这一想法虽然具有吸引力,却挑战了生物学的基本法则之一,也被称为“生物学的第二定律”, “Weismann障碍”:生殖细胞中的遗传信息与躯体影响是分开的。
因此,动物对环境的反应不应成为遗传。但是,在2019年6月7日,2篇Cell同时发表,挑战了这一法则,认为至少在线虫(C. elegans)这种模式生物中,记忆能够被遗传!而且,这样的遗传性可以维持3代到4代。
以色列特拉维夫大学Oded Rechavi团队在Cell 在线发表题为“Neuronal Small RNAs Control Behavior Transgenerationally”的研究论文,该研究发现秀丽隐杆线虫亲本的生物学反应可以传递可遗传的小RNA,其通过跨代方式调节基因表达。 神经元特异合成的小RNA调节生殖细胞的endo-siRNA和生殖细胞的基因表达,这可以维持多代。
此外,神经元中小RNA的产生通过生殖细胞Argonaute HRDE-1控制后代的趋化性行为至少三代。 在这些小RNA的靶标中,鉴定了保守基因saeg-2,其在生殖细胞中被隔代中下调。 因此,该研究提出了一种基于小RNA的机制,用于跨代传递神经元过程。
美国普林斯顿大学Coleen T. Murphy团队在Cell 在线发表题为“Piwi/PRG-1 Argonaute and TGF-β Mediate Transgenerational Learned Pathogenic Avoidance”的研究论文,该研究发现线虫不仅学会规避铜绿假单胞菌(PA14),而且通过感觉神经元中的生长因子β(TGF-β)信号传导和Piwi Argonaute小RNA途径,可以将这种规避行为传递给后代多达四代。
病原学规避的跨代表观遗传可能允许蠕虫在复杂的环境中生存,提高它们在规避疾病的同时获得足够营养的能力。

在身体的不同组织中,神经系统收集和组织环境信息的能力是不一样的。自从古代以来,许多人推测大脑活动可能以某种方式产生可遗传的变化,这将影响下一代的命运。神经系统可以控制后代的可能性可能会产生深远的影响。
然而,这一想法虽然具有吸引力,却挑战了生物学的基本法则之一,也被称为“生物学的第二定律”, “Weismann障碍(1891年提出)”断言,生殖细胞中的遗传信息与躯体影响是分开的。因此,动物对环境的反应不应成为遗传。更具体地说,如果“Weismann障碍”确实是不可渗透的,那么神经元活动的不应该影响后代。尽管如此,许多研究表明父母的神经元反应会影响后代的行为。虽然这些例子是令人着迷的,但确切的机制仍然是未知的。
在线虫中,来自人工,外源供应的双链RNA(exo-siRNAs)从体细胞(包括神经元)转移到生殖细胞。隔代基因调控依赖于RNA依赖性RNA聚合酶(RdRPs)扩增可遗传的小RNA,这些小RNA结合Argonautes,如HRDE-1(可遗传的RNAi缺陷1)。环境挑战(例如,饥饿和高温)调节可遗传的小RNA库并产生持续多代的反应。
像许多其他生物一样,线虫在体细胞和生殖中自然地产生内源siRNA(endo-siRNA),其与基因组中的多个基因座互补配对。 Endo-siRNA靶向蛋白质编码和非蛋白质编码基因座,进而调控其表达。
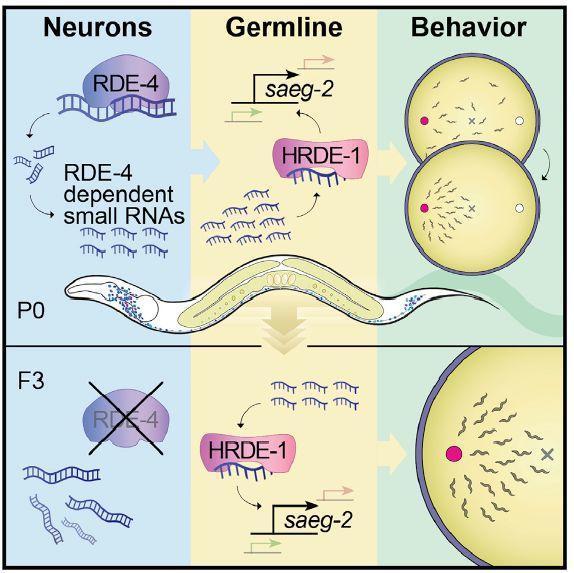
文章总结
目前尚不清楚神经系统的活动是否可以遗传。 在该研究中,秀丽隐杆线虫亲本的生物学反应可以传递可遗传的小RNA,其通过跨代方式调节基因表达。 神经元特异合成的小RNA调节生殖细胞的endo-siRNA和生殖细胞的基因表达,这可以维持多代。
此外,神经元中小RNA的产生通过生殖细胞Argonaute HRDE-1控制后代的趋化性行为至少三代。 在这些小RNA的靶标中,鉴定了保守基因saeg-2,其在生殖细胞中被隔代中下调。 因此,该研究提出了一种基于小RNA的机制,用于跨代传递神经元过程。

植物和动物的生理和行为特征受环境的影响很大。响应于环境变化的可塑性可以通过表观遗传学来控制。值得注意的是,表观遗传变化及其对基因表达的后续影响不仅限于单个生物体的一生,而且还可以在称为跨代表观遗传(TEI)的现象中跨越多代传播。
TEI已经被证明可以在重复元素(如转座子)的沉默和细胞应激的生理反应中发挥作用,如饥饿和渗透压。尽管在描述TEI及其分子组成部分方面取得了进展,但是TEI是否能够传达编码动物行为的信息以及哪些表观遗传机制是这些行为的基础,则不太了解。
秀丽隐杆线虫已经成为研究TEI的首要生物体,因为它具有极短的生存周期,大量子代和进化保守的表观遗传机制,可编码和传递跨代信息。此外,线虫不提供母体护理,亲本的微生物组不会在实验室环境中转移到子代 - 这两个因素可能会混淆哺乳动物TEI的机制研究。
RNAi在二十多年前首次在秀丽隐杆线虫中发现,后来被发现在许多物种中具有功能保守性,包括哺乳动物。随后,观察到由双链RNA(dsRNA)诱导的基因沉默可以在秀丽隐杆线虫中遗传3-20 代。
秀丽隐杆线虫栖息在多样的自然环境中,必须经常分辨营养和传染性细菌食物来源。事实上,~30%的秀丽隐杆线虫的天然微生物环境由假单胞菌属物种组成,其中一些是病原体。
尽管铜绿假单胞菌(PA14)在接触后数小时或数天内杀死秀丽隐杆线虫,但最初,线虫被PA14吸引 - 事实上,它们更喜欢非致病性实验室大肠杆菌(OP50) - 但是,在接触后数小时内,他们学会避免这种病原体。

总结
在这里,研究人员发现线虫不仅学会规避铜绿假单胞菌(PA14),而且通过感觉神经元中的生长因子β(TGF-β)信号传导和Piwi Argonaute小RNA途径,也可以将这种规避行为传递给后代多达四代。继承TEI编码行为的蠕虫能够规避致病细菌,这为它们提供了生存优势。病原学规避的TEI可能允许蠕虫在复杂的环境中生存,提高它们在规避疾病的同时获得足够营养的能力。
本文参考信息:
https://www.cell.com/cell/fulltext/S0092-8674(19)30448-9#
https://www.cell.com/cell/fulltext/S0092-8674(19)30552-5
(感谢您的关注,如需答疑请私信)
,




