心血管病风险在轻微肾损伤时就可以存在,在终末期肾病(ESRD)患者中风险最高,并且独立于其他风险因素。肾功能异常可以改变血脂的水平、组成和质量,易于导致动脉粥样硬化。现有证据表明,降低低密度脂蛋白胆固醇(LDL-C)有利于预防慢性肾脏病(CKD)患者和肾移植受者中的主要动脉粥样硬化事件,但对透析患者无益。
改善全球肾脏病预后组织(KDIGO)于2013年发布的《CKD 脂质管理临床实践指南》为 CKD 和 ESRD 患者血脂异常的治疗提供了简单的建议。5年来,在 CKD 血脂管理方面有无新的进展?来自英国伯明翰大学的 Charles J. Ferro 教授等人近期在《自然综述 - 肾脏病学》杂志上发表了一篇综述。
要 点
(1)心血管风险与估计肾小球滤过率(eGFR)之间存在独立的分级负相关关系。ESRD 患者发生心血管事件的风险极高;
(2)在 CKD 和 ESRD 患者中,脂质代谢紊乱表现为甘油三酯(TG)和氧化脂蛋白水平升高,高密度脂蛋白胆固醇(HDL-C)水平降低,但 LDL-C 水平通常是正常的;
(3)随着 eGFR 的下降,基于他汀类药物治疗的主要心血管事件的获益减小,对于透析患者的益处很少;
(4)肾功能恶化导致一种独特的心血管疾病表型,即心力衰竭和心律失常导致的心血管事件大于由于动脉粥样硬化导致的事件;
(5)几种治疗血脂异常及其相关风险的新疗法正在开发,这些药剂大多数都是生物制剂,生产成本非常高;
(6)目前支持在 CKD 或 ESRD 患者中使用新型降脂药物的证据有限,需要进一步研究这些疗法。
慢性肾病中脂蛋白代谢的紊乱

在内源性途径中,肝脏分泌富含 TG 的极低密度脂蛋白(VLDL)颗粒,其将 TG 转运至外周组织。由于 TG 被脂蛋白脂肪酶(LPL)水解,VLDL 颗粒的大小减小,成为中密度脂蛋白(IDL)颗粒,最后是 LDL 颗粒,其保留了相当大量的胆固醇。LDL 颗粒将胆固醇转运至肝脏和外周组织,并被 LDL 受体(LDLR)以及其他特异性受体和清道夫受体如清道夫受体 B1(SR-B1)清除。
在外源途径中,富含 TG 的乳糜微粒(CM)运输从肠道吸收的膳食脂质。CM 被 LPL 分解代谢,导致产生由肝脏、肌肉和脂肪组织吸收的游离脂肪酸。CM 的大小迅速减小,成为通过 LDLR 被肝脏吸收的乳糜微粒残留物。HDL 颗粒在胆固醇逆向转运过程中起关键作用,胆固醇转运将胆固醇从外周细胞(包括巨噬细胞和内皮细胞)转运到肝脏。随着肾功能下降,朝向尿毒症脂质谱发生逐渐的定量转变,其特征在于 TG 升高,低 HDL-C 和可变水平的氧化 LDL(ox-LDL)和氨基甲酰化 LDL(c-LDL)胆固醇。脂质谱还通过包括糖尿病和肾病综合征在内的合并症进一步修饰。与定量变化平行,脂蛋白颗粒的主要定性变化也使其更致动脉粥样硬化,包括氧化增加。
新兴的脂质修饰疗法
综述中除了介绍他汀类、贝特类(纤维酸类)、胆酸结合剂、以及欧米伽 -3- 脂肪酸对于血脂紊乱的治疗,还重点总结介绍了新兴的降脂治疗方法。

KDIGO指南的修订建议

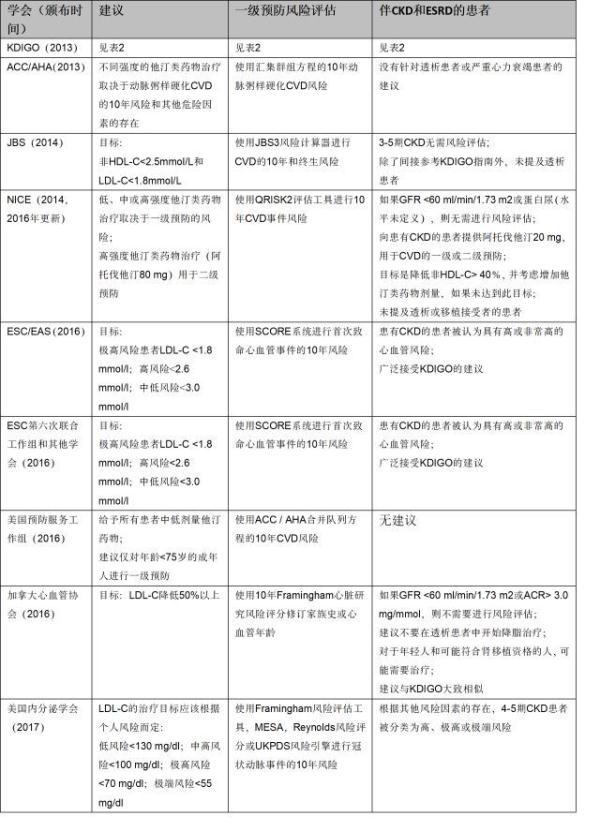
其他指南对于血脂治疗的建议
参考文献
Lipid management in patients with chronic kidney disease. Nature Reviews Nephrologyvolume 14, pages727–749 (2018)
编辑 | 徐德宇
版权声明:如涉及版权问题,请作者持权属证明与本网联系
,



