
电子式是表示微粒最外层电子结构的化学式。通常是在元素符号的周围,用小黑点“•”(或“×”)等符号表示元素的原子或离子的最外层电子个数。
用电子式可以表示原子、离子、单质分子,也可表示共价化合物、离子化合物及其形成过程。
书写电子式应该注意:
1. 无论何种微粒,其电子式都是由原子为基本单位组成的,不能出现角码甚至系数。
2. 组成各种微粒的各个原子的电子式,必须力求均匀、对称。稳定的8电子结构通常表示为四对电子(一般为元素符号的上、下、左、右各一对电子.)。
3. 电子式只能用示表示由主族元素形成的物质,不能表示由过渡元素形成的物质。

一. 原子:

依据元素的原子最外层电子个数的多少,先用小黑点“•”(或“*”)等符号在元素符号上、下、左、右各表示出1个电子,多余的电子配对。
例如:


二. 离子:

1. 阳离子:
简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就是其离子符号本身。
例如:
Na K Mg2 Ca2 Ba2 Al3
复杂的阳离子(例如NH4 、H3O 等.) 除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷。

2. 阴离子:
无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷。
例如:


三. 共价型单质分子:

必须正确地表示出共用电子对数,并满足每个原子的稳定结构。
例如:
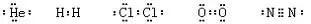

四. 共价化合物:

共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边。
例如:
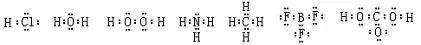

五. 离子化合物:

离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起。对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
例如:


六. 用电子式表示化合物的形成过程:

1. 共价化合物的形成过程示例:

2. 离子化合物的形成过程示例:


【知识拓展】

1. 共价键的三个参数
键能:指拆开或形成1mol共价键所吸收或放出的能量,单位:Kj/mol
键长:指成键原子的核间距离
键角:指共价键之间的夹角
规律:某共价键键长越短,键能往往越大,共价键就越牢固越稳定,破坏就越困难;
2. 对电子式的书写要掌握常见
原子(7个主族及0族)
离子(主族元素的简单阴、阳离子以及OH-、O2-、NH4 等)
单质(H2、O2、N2、卤素单质)
化合物[常见共价化合物如CH4、NH3、H2O、H2S、PH3、SiH4、HF、HCl、CO2、PCl3、H2O2、HClO、CCl4等;常见离子化合物如:NaCl、MgCl2、MgO、K2S、CaF2、Na2O2、NaOH、Ca(OH)2、NH4Cl、CaC2等]
基(简单的如—OH、—CH3、—NH2、—X等)等的电子式书写
▐ 标签:知识汇总
▐ 更多内容请关注微信公众号平台:高考化学 ID:gkhx100
,




