更多消息,请关注公众号--“康桥电池能源CamCellLab”
C博士专栏 ,专注于电池电化学领域的博士及专家们的专栏。本栏目特邀请公众号“康桥电池能源CamCellLab”的特约撰稿人查尔斯博士,他多年从事电池电化学方面的研究工作。去年他在本公众号开专栏,介绍电池知识,获得很好的反响。今年他开始介绍一些大学化学知识,非常精彩,看内容!

图1:乌克兰洞穴深处发现的石膏晶体
图1是在乌克兰洞穴深处发现的石膏晶体由 CaSO4·2H2O组成。钙离子和硫酸根离子在原子尺度上通过离子键结合,令人惊奇的是,这种原子尺度的离子键结合可以形成特征晶体形状,而被人类通过肉眼所识别。

图2:金属钠与氯气反应生成离子化合物氯化钠。
通过离子键结合形成的物质可以叫做离子化合物。通常是由元素周期表左侧的金属与右侧的非金属(不包括稀有气体有气体,第 18 族)相互作用产生的。例如,当金属钠 Na(s) 与氯气 Cl2(g) 接触时,会发生剧烈反应。这种放热的反应的产物是氯化钠,NaCl(s):
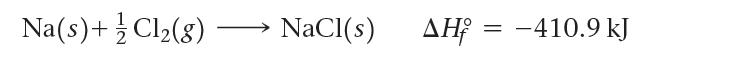
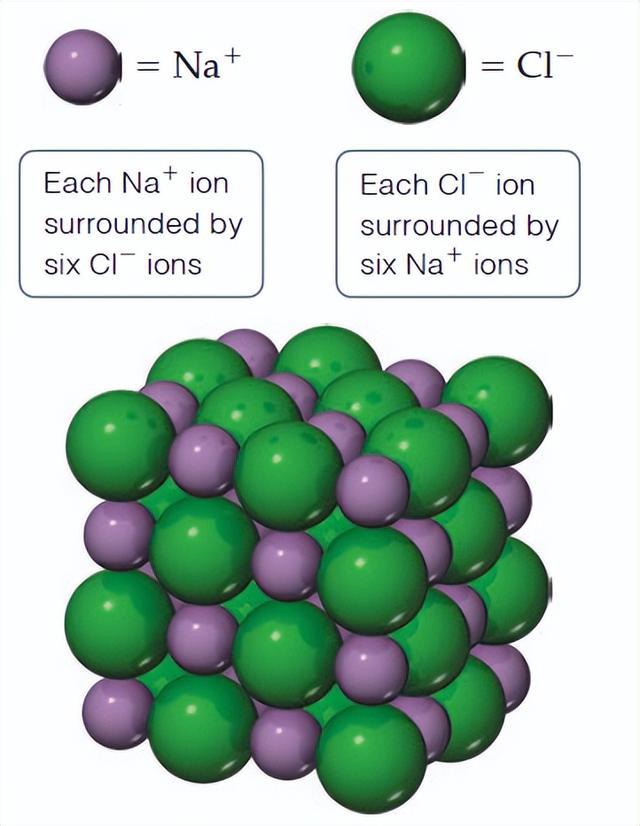
图3:氯化钠的晶体结构。
氯化钠由以三维阵列排列的 Na 和 Cl-离子组成。
从 Na 生成 Na 和从 Cl2 生成 Cl- 表明:钠原子失去了一个电子,而这个电子被氯原子得到了。也就是说,电子从Na 原子转移到 Cl 原子。原子有两个性质来表明电子转移的难易程度:电离能,表示电子从原子中移出的难易程度;电子亲和力,它衡量一个原子获得电子时释放的能量。
当一个原子很容易放弃一个电子(低电离能)而另一个原子很容易获得一个电子(高电子亲和力)时,就会发生电子转移以形成带相反电荷的离子。因此,NaCl 是一种典型的离子化合物,因为它由低电离能的金属和高电子亲和力的非金属组成。使用刘易斯符号,我们可以将此反应表示为
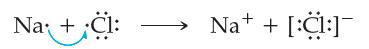
蓝色箭头表示电子从 Na 原子转移到 Cl 原子。每个离子都有一个八电子稳定结构,Na 的电子排列是2s22p6 ,也就是失去3s价电子后的电子构型。我们在氯离子周围放置了一个括号,以强调所有八个电子都位于它上面。
离子化合物具有几个特性。它们通常是具有高熔点的脆性物质。它们通常是结晶的。此外,离子化合物通常可以裂解,也就是说,它们沿着光滑、平坦的表面分开。这些特性是由静电力产生的,该静电力将离子保持在刚性、边界明确的三维排列中,如图 3 所示。
下期剧透:形成离子键的能量
,




