教科书教给我们一个知识:共价键是由成键的两个原子共享一个电子对形成的,每个成键原子贡献一个电子。那么,碳元素(C)有四个最外层电子,理应形成四个共价键。然而,事实并非如此。在20世纪70年代,德国科学家制备了一个被称为“六甲基苯”的分子(如图1所示)。在这个分子中,六个碳原子形成一个平面的六角环,环上每一个碳原子刮着另一个碳原子,而这个碳原子又和三个氢原子相连。这样,环上的碳原子形成了三个共价键,剩下的电子在环内自由运动。

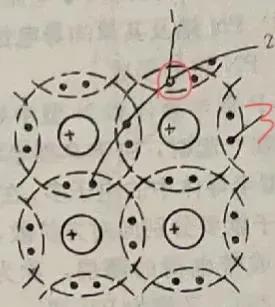
图2:新分子的结构
当然,需要指出的是,这并不是传统意义上认为的由两个电子形成的共价键;然而,它让人们对化学键有了新的认识。
,