第五单元 化学方程式
课题1 质量守恒定律(S14)
一、质量守恒定律
1. 概念:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和
例如:红磷在空气中燃烧,生成五氧化二磷,根据质量守恒定律,参加反应的红磷和氧气
的质量总和等于反应生成的五氧化二磷的质量。
2. 适用范围:化学变化(必考)
3. 实验验证:对有气体参加或有气体生成的反应,实验装置应密闭(必考)
微观解释:在化学反应中,反应前后原子的种类、数目和质量都没有变化。(必考)
4. 微观解释:在化学反应中,反应前后原子的种类、数目和质量都没有变化。(必考)

5. 涉及的几个化学反应(重点背记化学方程式和现象)
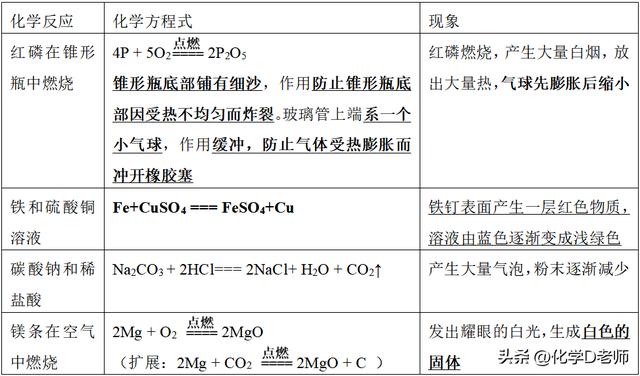
6. 化学方程式的4个意义(了解)
(1)表示反应物、生成物(2)表示反应条件
(3)表示各物质的质量比(4)表示各物质的微粒个数比
7. 化学方程式的三种读法,以2H2 O2 ==2H2O为例:
(1)宏观读法:氢气和氧气在点燃条件下反应生成水
(2)微观读法:在点燃条件下,每2个氢气分子和1个氧气分子反应生成2个水分子
(3)质量读法:在点燃条件下,每4份质量的氢气和32份质量的氧气反应生成36份质量的水
,




