当这场席卷全球的新型冠状病毒肺炎(COVID-19)发展进入到后疫情时代,如何快速现场鉴别诊断携带者和潜伏期患者,正成为当下新冠疫情防控的重点和难点。
华中科技大学生命学院刘钢教授团队利用其拥有的国际最新纳米等离子光学芯片专利技术,成功研发基于新型纳米等离子光学芯片技术的高灵敏度光学检测系统,可以快速特异性测量样品中的新冠病毒颗粒的浓度,使得新冠肺炎早期无症状感染现场快速无创检测成为可能。相关研究成果于10月15日以“One-Step Rapid Quantification of SARS-CoV-2 Virus Particles via Low-Cost Nanoplasmonic Sensors in Generic Microplate Reader and Point-of-Care Device”为题发表于Biosensors and Bioelectronics。Biosensors and Bioelectronics为国际工程科技类顶级期刊,中科院SCI期刊分区一区,最新影响因子为10.25,位于 ESI 前10%。论文第一作者是华中科技大学博士后黄丽萍博士。

图1. 纳米等离子光学传感芯片检测新冠病毒颗粒示意图
等离子共振分析测试及成像是无需荧光或染料标定的生物分子、病毒和细胞的实时分析测试技术。由于Nanoplasmonic Sensor芯片产品对表面电介质的折射率变化非常灵敏,从而不需要标记,就可以快速、实时、原位、无损、动态检测人体体液中的病毒颗粒和目标蛋白的浓度,且该项创新产品的检测系统结构简单,成本低,操作简便,使得等离子共振分子互作检测技术在病毒及蛋白检测体外快速诊断的应用领域有了质的飞跃,这将助力中国乃至全球生物检测和医药研发产业的发展。目前,新冠病毒核酸检测已广泛应用于新冠肺炎的临床检测和诊断。但是核酸检测要经过病毒灭活裂解,RNA提取和反转录,DNA扩增和荧光标记等多步骤,必须由技术熟练的专业人员在专业实验室内操作。后续检测部分也离不开实验室设备和高昂的人力成本。另一方面,现有的传统免疫层析技术病毒抗原蛋白的检测试剂盒准确率和灵敏度无法满足临床实际需求。作为新的检测技术,病毒颗粒检测是最直接最准确的检测方法,可作为补充核酸检测的快速初筛手段对较大量样本的进行现场即时评估。由于鼻咽拭子和唾液中新冠病毒浓度低,现有的其它检测方式如酶联免疫吸附检测成本高,速度慢,操作复杂且条件要求高,结果显示不够直观。
该研发团队研发了纳米等离子光学共振芯片,具有由介电材料所包围金属超材料纳米结构中的电子气体集体振荡产生的特殊光学性质。新型纳米等离子光学芯片不需要光学耦合器件配合激发且具有更高的共振模式品质,借助这种传感器芯片后仅用常规的普通设备如光学显微镜和酶标仪等就能完成病毒表面蛋白和抗体之间结合过程的定量分析测定。本方法采用普通酶标仪或自制便携式透射光强度检测系统,通过采集的透光率变化来定量分析待测体液中的病毒浓度。该项目采用普通酶标仪或自制便携式透射光强度检测系统,对新冠假病毒实现无标记的快速定量检测,实验结果表明目前该系统进行无标记新冠病毒定量检测的线性范围为10^2~10^7 vp/mL,最低检测限为370 vp/mL,这样的灵敏度可以满足唾液中的新冠病毒浓度快速检测(传染期感染者唾液中新冠病毒浓度为10^5至10^6 vp/ml)的要求。该检测手段有着无需标记、受背景影响小、高通量、线性浓度范围广的优点。同时,测试中还采用SARS、MERS以及VSV三种假病毒对该检测系统进行了特异性验证,结果发现该检测系统对新冠病毒检测具有1000:1以上的特异性,可实现新冠病毒颗粒的特异性结合与准确定量检测,对其它冠状病毒不敏感。
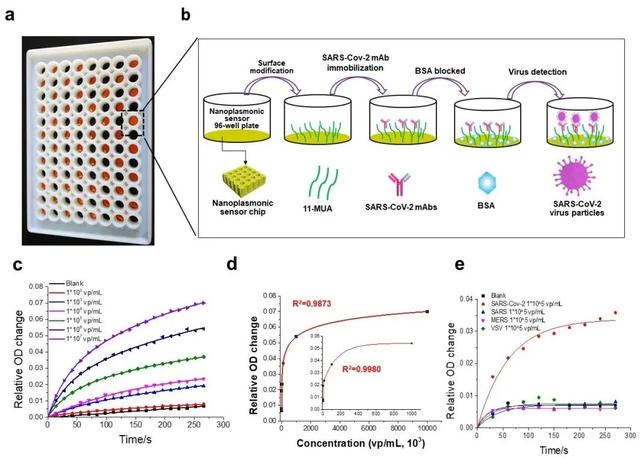
图2. (a)自制纳米等离子光学传感芯片微孔板示意图;(b)芯片修饰与病毒检测示意图;(c)新冠病毒颗粒定量检测动态曲线变化图;(d)新冠病毒颗粒定量检测标准曲线图;(e)新冠病毒颗粒检测的特异性验证图;

图3.(a)便携式透射光强度检测设备示意图;(b)便携式透射光强度检测设备检测病毒样本示意图;(c)便携式透射光强度检测设备检测新冠病毒颗粒的动态变化曲线;(d)便携式透射光强度检测设备对新冠病毒检测特异性验证图。
该研究联合我校生命学院、量准实业有限公司、武汉新芯集成电路制造有限公司,台积电和上海公共卫生临床中心等国内产、学、研、医行业多家单位共同参与研发。该研究有望实现用唾液进行新型冠状病毒肺炎快速检测技术并生产可以在临床和居家使用的超快速检测唾液中新型冠状病毒颗粒浓度的测试产品及相应的手持式数字化分子检测设备,为新冠肺炎疾病的快速诊断提供帮助。人民日报社前期也对该研究做了相关报道。
来源:华中科技大学
原文链接:
https://www.sciencedirect.com/science/article/pii/S0956566320306746?via=ihub
https://doi.org/10.1016/j.bios.2020.112685
,