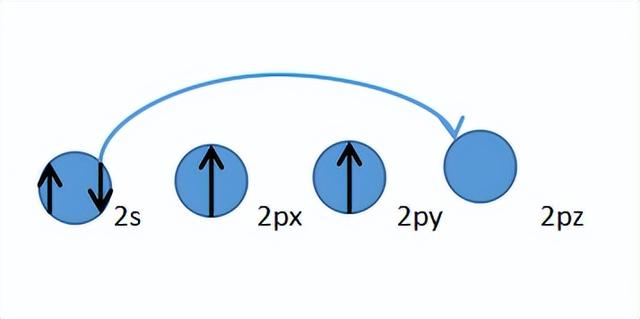
水的两个氢原子被烃基取代的有机物为醚,醚的官能团是醚键(-O-)。
常见的醚有乙醚,乙醚沸点很低,使用时不能用到明火,否则就会发生爆炸。
醚的分类两个取代烷基相同时称为对称醚,不同时称为混合醚。常见的对称醚有甲醚、乙醚,混合醚有甲基乙基醚。这类醚的命名也是先读出两个取代基后面再加一个“醚”字。

按照两个取代基的类别,将其分为脂肪醚和芳香醚。

根据醚分子中有无环,还可以分为环醚和无环醚。如果环上患有氧原子,那么就成为环氧化合物。

醚的熔沸点都比较低,因为它不能像醇分子一样形成分子间氢键,所以醚的沸点要比同碳数的醇低的多,如甲醚的沸点为-25℃,而乙醇的沸点为78℃。
对于与水的互溶性,大部分醚都是不溶于水的,但四氢呋喃和1,4-二氧六环却能与水完全互溶,这是由于一般醚的氧都被旁边的氧包围起来了,难以与水形成氢键。而四氢呋喃和1,4-二氧六环的氧被裸露出来,与水形成氢键,增加了与水的相容性。
醚的结构醚的氧原子SP3杂化,氧原子的两队孤对电子分别占据两个SP3杂化轨道,另外俩个SP3杂化轨道分别去邻位碳原子的SP3杂化轨道重叠形成σ键。由于σ键的键能较大,破坏起来比较难,所以醚是一个比较稳定的有机物。
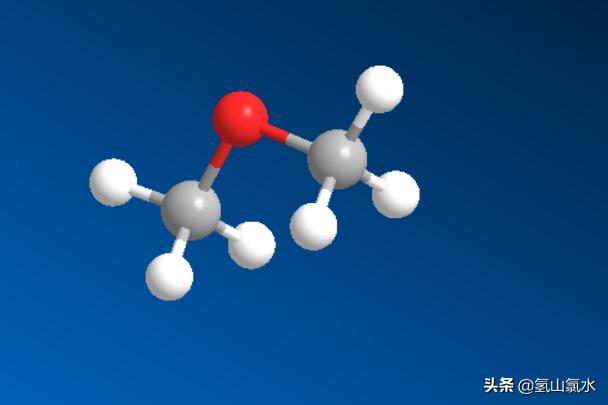
甲醚的球棍模型

乙醚的球棍模型
醚的化学性质前面介绍了醚的结构,结构决定性质,性质决定用途。醚的结构就说明醚的最容易短的键是碳氧键,因为碳氧的电负性相差较大。
(1)烊盐的形成
由于醚键的氧有孤对电子,所以它可以相当于路易斯碱,即可以与硫酸、盐酸或路易斯酸形成烊盐。

(2)醚的碳氧键断裂的反应
醚在HI中加热,容易发生碳氧键断裂的反应。反应中,氢离子先与氧原子形成烊盐,然后根据醚的结构,发生SN2或SN1反应。一级烷基容易发生SN2反应,3级烷烃容易发生SN1反应,生成物是对应的醇和碘代烷,如果反应体系酸过量,醇会继续反应生成卤代烷。

对于混合醚,碳氧键断裂的顺序为:三级烷基>二级烷基>一级烷基。
环醚的开环反应(1)酸性条件下开环
当有机物的环中含氧原子时,为环醚。环醚的碳氧键也可以断,在酸性条件下,氧原子被质子化,带一个正电荷,对与其相连的碳原子周围的电子有吸引作用,使碳原子带有部分正电荷,当亲核试剂进攻时,增强了与亲核试剂的结合能力。
那么,亲核试剂进攻哪一个碳呢?这取决于哪个碳原子的正电性大,即连取代基较多的碳,因为取代基一般是给电子基团,有利于碳正离子的稳定性。如下图中亲核试剂进攻红色碳。

(2)碱性条件下开环
碱性条件下的开环,主要靠亲核试剂的进攻,所以碱性开环时要求亲核试剂的亲和性要强。此时,断开哪一个碳氧键取决于空间位阻。在大多情况下与酸性条件下相反。

键的形成与断裂同时发生
醚的制备现在有机合成方法中合成醚的方法较好的是Williamson合成法。
Williamson合成法是利用醇和卤代烃在无水条件下的反应。
RONa R'X ---------- ROR' NaX
由于这是一个SN2反应,醇钠的烷氧负离子作为亲核试剂希望其亲和性较强,而被进攻的卤代烃希望其空间位阻较小,所以氯代烃最好是一级卤代烃。
总之,醚类化合物利用其稳定性,可做反应溶剂。环氧乙烷类化合物也是合成高分子化合物的构造单元。同时,冠醚类分子(如18-冠-6)可做相转移催化剂。
根据相似相溶原理,有机物易溶于有机溶剂,所以有机反应一般用有机溶剂做反应溶剂,无机反应一般用水作溶剂。那么,如果想让有机物和无机物反应怎么办呢?这是就需要像反应体系加相转移催化剂。相转移催化剂就像搬运工一样,将水相的无机物搬到有机相让他们反应,然后再返回水相继续搬运,所以,反应加入一点就可以了。
,