
第一作者:Bairav S. Vishnugopi
通讯作者:Md Toukir Hasan,Hanwei Zhou,ParthaP. Mukherjee*。
单位:Purdue University
界面和电极串扰决定了固态电池的热稳定性
随着锂离子电池(LIBs)接近其理论能量密度,它们面临着有关安全和耐久性的挑战。由于锂(Li)金属阳极的低电化学电位(与标准氢电极相比为-3.04V)、高比容量(3860 mAhg–1 )和低密度,利用它们是提高锂离子电池能量密度的一个有希望的方法。然而,金属锂的高反应性,导致枝晶生长和内部短路,仍然是一个主要的安全问题,大多数液体电解质的可燃性加剧了这一问题。在这方面,使用不易燃的无机固体电解质(SE)的固态电池(SSBs)的发展被认为是实现锂金属阳极和改善热安全性的重要一步。尽管有SE的前景,但在广泛的SSB系统中观察到的金属锂的形态不稳定。例如,Li7La3Zr2O12(LLZO)、Li6PS5Cl(LPSCl)、Li3PS4(LPS)一直面临瓶颈。
为了了解锂枝晶的起源,各种可能机制,包括界面接触的丧失,晶界和表面缺陷已经被探测到。此外,在与金属锂接触时,基于氧化物和硫化物的SE的热力学不稳定性质会导致界面的形成。界面生长已被确定为SEs的一个关键失效机制,如Li1.4Al0.4Ge1.6(PO4 ) 3(LAGP)和Li10SnP2S12(LSPS) 。虽然主要重点放在电化学机械、形态学和传输限制上, SSB的热安全性,已经被最近的一些研究提请注意,仍然需要进行严格的调查。除了不可燃性转化为热安全性的传统观念外,还需要建立固-固界面的电化学/化学特性与其热稳定性之间的基本映射关系。
金属锂的高反应性和低熔点,加上SE/Li界面的电化学演变(例如,界面生长)是在热安全方面仍需审视的关键方面。SSB的热稳定性有可能取决于内在固-固界面上发生的不同的电化学相互作用和降解过程。此外,滥用情况,如外部加热和内部短路(例如,由于锂丝穿透),这涉及到电化学能量转换为热量,可能会导致内部温度升高。因此,对于给定的电极和电解质材料的组合,当务之急是量化临界温度极限,超过这个极限,SSB就会发生热失控。认识到潜在的机理相互作用,材料层面和电池层面的热稳定性之间的差距也应该被弥合。
【工作介绍】
本工作研究了三种广泛使用的硫化物电解质,即LPS、LPSCl和LSPS与金属Li之间的界面特性和热稳定性之间的基本关联。使用加速率量热法(ARC)研究它们的热稳定性,虽然LPS/Li和LPSCl/Li界面在电化学循环前后表现出类似的放热行为,但LSPS/Li界面却表现出明显不同的反应。即使在未循环状态下,LSPS/Li界面也会发生热失控,并且在循环后明显加剧,这伴随着在Li熔点附近出现的巨大热峰值。X射线光电子能谱(XPS)分析揭示了热失控开始的这种转变与涉及金属锡形成的LSPS界面的演变之间的独特联系。

此外,开发了一个计算模型,在观察到的材料级反应的基础上捕捉到电池级的热稳定性,并划定了作为界面/锂相互作用、阴极/锂串扰和特定能量函数的安全制度图。分析表明,虽然SSBs需要比LIBs更大的温度才能发生热失控,但超过这个限度,它们就会出现严重的自热率和温度上升。随着SSB的研究继续揭开界面退化的各种模式,本研究强调了同时评估其对安全的影响的关键需要。
【具体内容】
热力学上稳定且无反应的SE/Li界面不涉及固体电解质界面(SEI)的形成。然而,大多数SE与金属锂在热力学上是不稳定的,这导致了SE的分解和界面的形成。当界面表现出可忽略的电子传导性和足够的离子传导性时,它在动力学上是自限的(图1a,b)。然而,离子-电子混合导电界面(MCI)的形成会导致界面持续增长(图1a,c)。在进行热稳定性分析之前,研究了对称的Li/SE/Li(SE=LPS,LPSCl,LSPS)电池的电化学反应。对称电池在0.1 mAcm–2 ,总容量为10 mAh cm–2 。在0.1 mAcm–2 ,Li/LPS/Li电池显示出相对稳定的循环,持续时间为100小时,每次循环的过电位没有明显变化(图1d,e)。沿着Li/LPSCl/Li电池的类似路线,每个周期的过电位趋势几乎保持不变(图1f)。由于界面接触的丧失,在每个半周期内观察到电池极化的增加∼5 mV(图1g)。相比之下,Li/LSPS/Li电池在20小时内显示出0.8V的过电位增加,100小时后为2.7V(图1h,i)。循环前后的EIS光谱的比较表明了一个明显的阻抗上升(图1j)。循环中阻抗的增加可能是由于在LSPS/Li界面的界面生长,这导致了离子传输的额外阻力。与此相关,LSPS/Li界面上活性接触的丧失也可能是阻抗上升的一个因素。空隙的形成会增加界面上的反应过电位和传输阻力。LPS/LPSCl/LSPS电池之间的过电位特征的差异表明,虽然LPS和LPSCl可以涉及动力学稳定的界面,但LSPS表现出渐进的界面增长。

图1.Li/SE/Li系统的电化学反应。(a)SE/Li界面可以涉及以下类型的界面:(b)动力学上的自限性界面和(c)离子-电子混合导电界面。(d)Li/LPS/Li、(f)Li/LPSCl/Li和(h)Li/LSPS/Li电池在0.1 mAcm–2 (总容量=10 mAh cm–2 )的恒流循环。(e,g,i) 放大图显示了循环早期阶段的过电位特征。(j) 循环前后Li/LSPS/Li电池的阻抗光谱。
在ARC测试中,使用加热-等待-寻找(HWS)方法,将样品以5℃的增量加热到400℃。在HWS过程中,初始温度为50℃,在各温度增量之间使用20分钟的等待时间。在等待步骤之后,如果在寻求步骤中发现由于自热而导致的温度上升(dT/dt)大于0.02 °C/min,ARC试验室将切换到绝热模式,并跟踪样品温度的上升,直到达到最高温度限制。热反应是以四个特征温度来量化的,其中包括Li熔化后出现第一个放热的温度(T0 ),由于自热而出现的连续放热的起始温度(T1 ),热失控的起始温度(T2 ),以及样品达到的最高温度(T3 )。每个样品由四个具有相同电化学性能的电池组成,以获得ARC测试中检测放热所需的热质量。通过这一分析,目标是回答两个问题:(1)在未循环状态下,LPS、LPSCl和LSPS与金属锂的界面是否会发生热失控?2)电化学循环或降解(例如,由于界面生长)是否会改变界面的热稳定性?
如图2a所示,未循环的LPS样品在296.5℃时显示出自热开始(T1 ),在349.6℃时出现放热(T2 )。超过这个极限,自热速率有相当大的增加(高达8.032 °C/min),这导致放热和最高温度为427.7 °C(图2a,b)。在Li熔化后,循环的和未循环的样品之间引发了热反应的小变化。然而,与未循环的样品相比,循环的LPS样品在特征温度和(dT/dt)方面几乎没有变化max ,这在表1中进行了总结。同样,在LPSCl的情况下,未循环的样品在185.8和275.7°C表现出两个主要的放热现象,如图2c所示。在循环和未循环的LPSCl样品之间,没有观察到特征温度和自热率的明显变化(图2c,d)。有趣的是,即使在LPS和LPSCl的情况下,也只检测到热反应的小差异(表1)。较小的放热(在185和190℃之间)可能是由于熔融锂和界面产物之间的反应,而较大的放热(在275和300℃之间)可能对应于界面的热分解及其随后与熔融锂的反应。

图2.探究SE/Li界面的热稳定性的ARC实验。(a)Li/LPS/Li,(c)Li/LPSCl/Li, 和(e)Li/LSPS/Li 对称电池在电化学循环前后的温度响应。(b)Li/LPS/Li、(d)Li/LPSCl/Li和(f)Li/LSPS/Li情况下的温度上升和相应的自热率。在循环后的LSPS/Li界面上观察到了一个急剧上升的自热率和一个由此产生的热失控起始点的转变。
表1.通过ARC实验量化的SE/Li界面的热特性

与LPS和LPSCl的情况相比,即使对于未循环的LSPS样品,也观察到了截然不同的放热反应,它在295℃时表现出一个大的热峰值(图2e)。检测到一个明显较高的自热速率(高达196.3 °C/min),这导致了热失控和最高温度412.7 °C(图2e,f)。在这项研究中,自热率大于60 °C/min被用作划分热失控的标准。耐人寻味的是,循环的LSPS样品中的热失控行为更加严重,从而显示出在锂的熔点附近的巨大温度峰值。如图2e所示,自热的开始发生在177.1℃,并导致193.6℃的放热。此外,自热速率上升到19652.2℃/分钟(图2f),这导致最高温度为505.4℃。可以注意到,由于在ARC测试过程中没有电流通过,所获得的热特征归因于界面的化学成分,而不依赖于电池电阻。因此,循环和未循环样品之间的任何界面成分的变化应该表现为不同的热反应。根据在未循环/循环的LPS、LPSCl和LSPS情况下检测到的ARC特征,LSPS在电化学循环过程中可能涉及一种新的分解产物。即使这种分解产物是热稳定的,它也有可能作为一种催化剂,导致另一种成分的分解,从而在界面上产生放热作用。
通过对(i)SE与金属锂接触24小时的样品(未循环电池)和(ii)在0.1mA cm–2 ,容量为10mA cm–2 (∼100小时)的电化学循环的样品进行XPS实验,可以了解界面组成。对于未循环的LPS样品,从S 2p和P 2p光谱中,检测到Li2S(160 eV)、Li3P(126.8 eV)和还原磷化合物(131 eV)的形成(图3a)。在电化学循环后,这些峰值已经衰减,在XPS光谱中没有观察到(图3a),这也表明LPS不会发生连续的分解。与金属锂接触后,LPSCl分解为Li2S(159.9 eV)、Li3P(126.7 eV)和还原磷成分,如图3b的XPS光谱所见。与以前的研究一致,LPSCl和LiCl中的Cl– 之间的结合能差很小,因此很难确定LiCl的存在。对于循环的LPSCl样品(图3b),虽然Li2S峰的强度有很大的下降,但没有观察到对应于Li3P和还原磷成分的峰,从而表示夹层的非渐进性质。XPS实验中观察到的LPS/Li和LPSCl/Li界面的分解产物与之前的理论预测是一致的。由于循环/非循环的LPS和LPSCl样品显示出几乎相同的热反应(表1),观察到的放热(图2a,c)可能是由于共同产物之一的热分解。此外,导致放热的共同产物的数量也应该非常接近。由于LPS和LPSCl的相位不会随着循环而增长,所以由于这些共同产品之一而产生的放热源可能是有限的。虽然这种常见的产物有可能是Li2S、Li3P或还原的磷成分,但随着Li金属的反复电镀和剥离,它们会被埋在界面上。这与循环后这些成分的峰值强度降低有关。除了这些分解产物,P-S-Li硫成分和对应于PS43– 的磷成分是循环前后的常见成分(图3a,b);这些成分可能是导致观察到的放热的潜在可能。

图3.电化学循环前后的SE分解产物的比较。(a)LPS/Li界面的S 2p和P 2p核心区;(b)LPSCl/Li界面的S 2p、P 2p和Cl 2p核心区;以及(c)LSPS/Li界面的S 2p、P 2p和Sn 3d核心区。(d)LSPS/Li界面的界面演变,在循环过程中导致了Sn的形成。这种化学成分的变化显示出与LSPS/Li界面的热失控开始有明显的关联,它随着循环从295℃下降到193.6℃。在(a-c)中,还原的P表示还原的磷成分,在(c)中,Li-Sn是指Li-Sn合金。
当LSPS与Li接触时,从S 2p和P 2p光谱中确定了Li2S(159.8 eV)、Li3P(127.5 eV)和还原磷成分(129.9 eV)的形成(图3c)。从Sn 3d光谱中,检测到一个493 eV的峰值,根据理论预测,它应该对应于Li17Sn4 。因此,LSPS中的Sn4 被还原成Li-Sn合金,这就是化学相的电子导电性能的原因。与LPS和LPSCl相位相比,Li-Sn合金在未循环的LSPS相位中是一种独特的成分。有趣的是, ARC结果与这种成分差异相关,也表示了热反应的明显变化。与LPS/LPSCl样品(图2b,d)相比,未循环的LSPS样品(图2f)显示出超过20倍的自热率,同时还出现了热失控。结合从ARC反应和界面成分中得到的启示,界面中Li-Sn合金的存在可以影响未循环的LSPS/Li界面的热不稳定性。虽然锂-Sn合金本身可以是热稳定的,但在达到一定温度后,它可以促进另一个成分的形成或分解,这反过来可能导致界面上的放热作用。未循环的LSPS样品的这种放热的表现,与LPS和LPSCl样品不同,突出了界面作用和热稳定性之间的基础关联。
与LPS和LPSCl相反,对于LSPS样品,循环后仍然可以看到Li2S、Li3P和还原磷成分的峰(图3c),这表示界面的连续生长。除了Li-Sn合金,在Sn 3d光谱中还观察到一个新的峰值(图3c),它与金属Sn的结合能(484.6 eV)显示出很好的一致性。因此,与化学界面(未循环情况)相比,在电化学循环过程中,LSPS中的Sn4 进一步减少为金属Sn。界面成分的这种差异也显示出与热特征的有趣关联(见图2e)。未循环的LSPS样品的热失控发生在295.0℃,而循环的LSPS样品的热失控发生在193.6℃,伴随着自热率和最高温度的急剧增加。根据ARC和XPS的综合观察,推断出LSPS界面的演变与180℃附近的放热反应有关。由于Li-Sn/Sn成分的电子传导性,它们的存在导致了界面的持续增长,这影响了界面上的放热程度。此外,尽管循环的LSPS界面中的金属锡可以是热稳定的,但它可以作为催化剂,促进另一个成分的分解,反过来影响放热反应的开始。总的来说,LSPS界面在循环前后的基本差异与ARC实验中观察到的明显不同的热反应相吻合。图3d显示了所提出的LSPS/Li界面的热稳定性-界面关系的示意图。
从ARC实验中获得的材料层面的热特征(图2)为SE/Li界面的放热反应动力学提供了重要的洞察力。ARC曲线中从温和放热(从T1 )到热失控(直到T3 )的过渡阶段可以用来提取动力学参数[即活化能(Ea )、频率因子(A)]和反应焓(H),这些参数与每个SE/Li界面的放热反应相对应,基于方程式S1和S2。根据ARC实验捕捉到的热反应(图2),未循环的LSPS/Li界面的放热严重性通过与这种热相互作用相关的增强的频率因子(A)来说明。从物理上讲,未循环的LSPS样品从T1 到T3 的ARC特征表示界面上有很大的放热反应速率。至于循环的LSPS/Li界面,大的放热反应速率也伴随着高的反应焓。这些热动力学参数的共同影响与ARC实验中观察到的循环LSPS样品明显较高的温升和自热率有关(图2e,f)。与ARC的特征相一致,LPS和LPSCl样品涉及与电化学循环前后的放热作用有关的类似动力学参数。根据SE/Li界面的热反应,开发了一个计算模型来捕捉电池水平上的温度上升和自热特性。以LiCoO2 (LCO)作为代表阴极。对于LCO阴极,氧气释放和与Li反应的差示扫描量热法(DSC)热流数据被用来划定相关的动力学参数。如公式1-3所示,SE/Li界面的热动力学和LCO/Li的相互作用被用来预测电池水平的热行为。

这里,Qgen 是总发热率,mi 是反应物质量,qi 是反应的比热,m是电池质量,h是总体传热系数,A是电池表面积,T是电池温度,TARC 是ARC室的温度,T0 是初始电池温度。根据SE,电池级的热稳定性在力学上受到固-固界面上热相互作用的不同性质的影响。
首先用LSPS作为SE进行分析。对于未循环的LSPS电池,如图4b所示,在255.0℃时只观察到一个放热阶段。从物理学上讲,这标志着以下机制。由于氧气从LCO阴极释放并与Li反应而导致的自热的开始,先于由于LSPS/Li界面的自热的开始。然而,由于氧的释放及其与Li的反应而产生的自热速率导致温度立即上升(1683.6℃/分钟,见图4c),这足以引发SE/Li界面的大规模放热反应(发生在326.9℃)。由于这两个反应之间的时间间隔在几秒钟之内,由于这两个相互作用而产生的热反应被观察为一个单一的峰值,这导致最高温度为748.0 °C。然而,对于循环的LSPS电池来说,由于LSPS/Li界面产生的热量首先出现在170.0℃(图4c)。产生的热量触发了LCO阴极的热分解,并导致随后在261.0℃开始出现放热,如图4b所示。相反,对于未循环的LSPS电池,186.5℃的温和放热(见图2e)不足以触发LCO的热分解。总的来说,虽然由于SE/Li间的热相互作用影响了阴极的反应,但在阴极释放的氧气也影响了随后在阳极产生的热量(图4a)。把这种机理上的互动称为 "电极串扰",它制约着热失控的发生和严重程度。图4d总结了由于SE/Li界面和LCO的氧气释放而产生的热量,从而揭示了后者机制的重大贡献。在图4d中,LIB和LMB指的是锂离子电池和液基锂金属电池。直方图中的橙色、绿色、红色、紫色、蓝色和黄色部分指的是SEI分解、阳极-电解质相互作用、阴极-电解质相互作用和电解质分解(对于LIB/LMB情况)以及SE/Li界面和Li/LCO相互作用(对于SSB情况)。由于金属锂电极与SE分解产物和氧气的高度放热反应,推断SSB中产生的总热量是LIB中产生热量的3倍以上(图4d)。
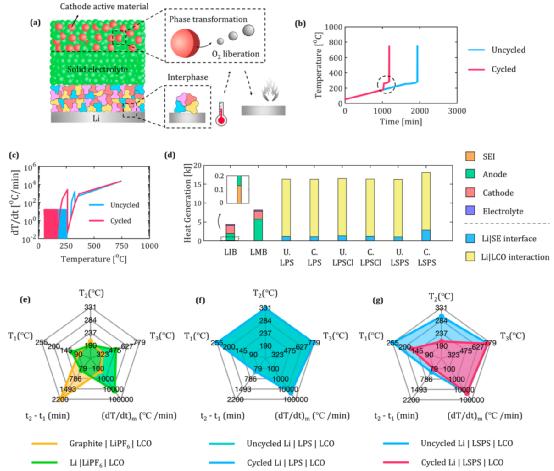
图4.电池的热稳定性。(a) 热失控机制,包括界面/锂的相互作用、O2 的释放及其与锂的反应,对于锂|LSPS|LCO电池。(b,c) 1安培锂|LSPS|LCO电池的温升和自热率。(d)LIB(石墨|LiFP6 |LCO)、LMB(Li|LiFP6 |LCO)和SSB(Li|SE|LCO)电池的发热量比较。这里,U.和C.分别指未循环和循环的。(e)LIB和LMB,(f)未循环和循环的基于LPS的SSB电池,和(g)未循环和循环的基于LSPS的SSB电池的热安全特性。
图4(e-g)中的蜘蛛图总结了LIB(带石墨阳极)、LMB和以LCO为阴极的1Ah容量的SSB的五个关键热安全属性。这里,(t2 - t1 )表示T1 和T2 之间的时间间隔,(dT/dt)m 表示最大温升率。
LIB和SSB之间存在三个主要区别:(1)LIB的自热(T1 , 90 °C)和热失控(T2 , 205 °C)的起始温度(图4e)比任何SSB的情况(图4f,g)都低。(2) 然而,SSB的(t2 - t1 )明显低于LIB。这在物理上是指SSB在T1 之后有更高的自热率。(3)最后,与LIB相比,SSB的(dT/dt)m 和最高达到的温度(T3 )要大得多。例如,LIB和SSB的T3 ,分别为323℃和744-779℃。总的来说,这意味着虽然SSB需要更大的温度来启动热失控,但一旦达到这个极限,自热率和温度上升是非常严重的。此外,从图4g可以看出,在像LSPS这样的SE中,由于界面生长造成的降解在决定热失控的发生方面起着关键作用。
由于SSB的温度上升幅度很大,因此了解能量释放的极限和可能导致热失控的加热情况非常重要。在这种情况下,一个关键的考虑因素是发生内部短路,导致储存的电能转换为热能。例如,在各种SE中,包括像LPS、LPSCl和LSPS这样的硫化物,已经观察到了因灯丝生长而发生的短路。电池的安全性,在应对短路时,取决于(i)比能量(Eg ),(ii)在正常电池操作期间发生的温度上升(Tcell operation),以及(iii)导致热失控的自我加热的起始温度(T1 )。在数学上,这些影响可以被归纳为安全系数(fsafety),其定义为

其中fsafety代表Eg的最小部分,需要转化为热量才能达到T1 ,并导致热失控,cp 表示电池比热。通过建立一个耦合的热电化学模型来评估Tcell operation,该模型可以捕捉到欧姆热(Qohmic = kSE ∇ ΦSE ∇ ΦSE )和动能热(Q̇kinetic = jreactionη)对电池运行期间内部温度上升的影响。这里,kSE 是SE 的离子传导率,ΦSE 是离子传输的电动势,jreaction 是反应电流密度,η 是过电位。T1 是从ARC结果中得到的。在公式4的基础上,评估了基于LSPS的SSB电池的fsafety(图4g)。如图5a所示,内部温升(ΔT)随着充电电流和比能量(Tcell operation,max = Tambient ΔT)的增加而升高。此外,比能量对公式4中的fsafety构成直接限制。因此,在未循环的情况下,随着比能量从200Wh/kg增加到300Wh/kg,fsafety从0.3下降到0.2∼(图5b)。此外,图5b还意味着随着电流密度的增加,安全系数也会降低。最重要的是,观察到循环电池的安全系数急剧下降,这归因于T1 的较低值(图5c)。因此,SE/Li界面的界面演变对SSB的电池级热安全有深刻的影响。

图5.SSB的安全状况。(a)电化学操作过程中的内部温度上升是比能量和充电电流密度的函数。(b)未循环和(c)循环的基于LSPS的SSB电池的安全系数(fsafety)评估。(d)Sankey图说明了影响SSBs中耦合安全降解反应的机械相互作用。
这项工作对界面特性和电极串扰对固态电池热安全的影响提出了基本的见解。对三种典型的硫化物,即LPS、LPSCl和LSPS,研究了SE/Li界面的热特征和界面演变之间的基本联系。重要的是,本工作发现,虽然LSPS/Li界面即使在未循环状态下也会表现出热失控,但电化学循环大大加剧了这种行为,这导致在Li的熔点附近出现巨大的热峰值。根据这些材料层面的特征,开发了一个计算模型来探测电池层面的热反应,并划定安全图作为SE/Li界面、电极串扰和比能量的函数。
在这项研究的推论基础上,提出了对SSBs安全和降解反应的复杂耦合的机理观点(图5d)。虽然内在的SE/Li界面对界面生长机制起着关键作用,但评估外在因素,如压力和温度对界面特性和热稳定性的潜在影响,可能是未来研究的一个重要途径。与SE/Li界面类似,了解阴极中SE的分解和相关的界面行为如何影响热安全也是至关重要的。除了在SE的不可燃性方面的典型安全描述外,本工作研究表明在固-固界面的电-化学-机械性质和它们的热稳定性之间建立一个全面的关联的必要性。
Interphases and Electrode Crosstalk Dictate the Thermal Stability of Solid-State Batteries
ACS Energy Letters ( IF 23.991 ) Pub Date : 2022-12-06 , DOI: 10.1021/acsenergylett.2c02443
Bairav S. Vishnugopi, Md Toukir Hasan, Hanwei Zhou, Partha P. Mukherjee
https://doi.org/10.1021/acsenergylett.2c02443
,




