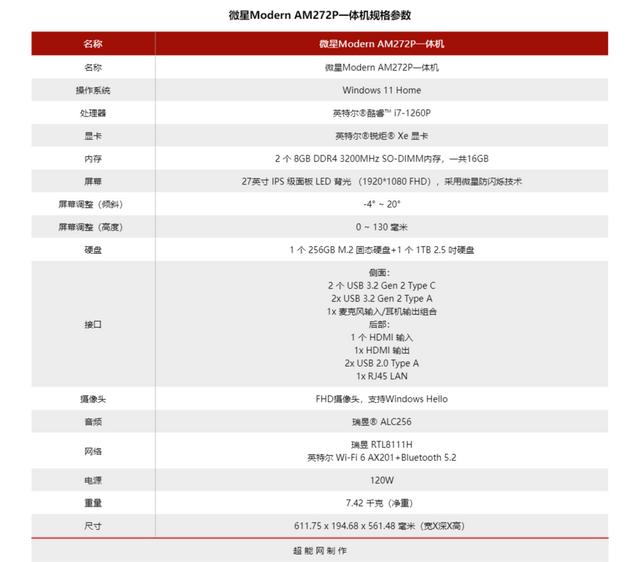
大家好,今天我们要一起来学习非常关键的内容,速率和平衡的图像问题。
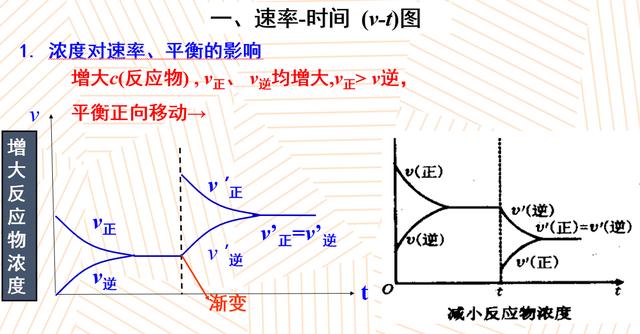
先为大家介绍第一部分,速率时间图,也就是我们常说的V-t图。能够影响速率的因素无非有浓度、温度、压强、催化剂、表面积等等,但是能够影响平衡移动发生的因素只有温度、浓度和压强这三个因素,所以我们先来看一看浓度对速率和平衡的影响。
当我们增大反应物浓度的时候,会观察到V正和V逆都是在变大的,那就说明旧的平衡被破坏,建立了一个新平衡的过程,直到新的V正和新的V逆相等。所以在我们增大反应物浓度的时候,正反应和逆反应的速率都是变大的。
由于正向速率它大于逆向速率,所以平衡会向着正向移动。对应的,如果减小反应物的浓度,我们会观察到正反应的速率在减小,逆反应的速率也在减小。但是正反应速率减小的程度会比逆反应速率减小的程度,继而达到一种新的平衡状态。
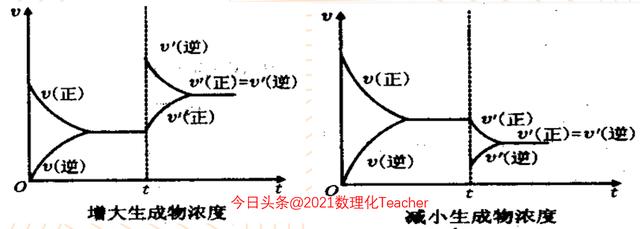
那如果我们增大生成物浓度呢,这时候我们就看到增大生成物浓度会使得逆反应的速率大于正反应的速率,而减小生成物的浓度会使得逆反应的速率减小。

将这四幅图共同展示在屏幕上方,大家就能够有一个清晰的、直观的认识,比如增大反应物浓度或者减小生成物浓度,都能够使化学平衡向着正、反方向移动,但是它们的图像是有很大的差异的。同理,减小反应物浓度或增大生成物浓度,化学平衡都会向着逆反应的方向移动,但是它们的图像依然是有很明确的差异。
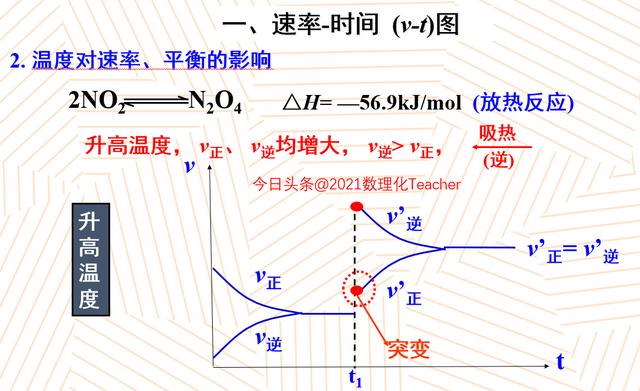
第二个因素,我们要来探讨温度对速率平衡的影响,依然是以二氧化氮和四氧化二氮的平衡体系为例,这是一个典型的放热过程,在升高温度的时候,我们会观察到温度升高正和逆的速率都会增大,但是由于这是一个放热的过程,所以V正和V逆,变大的趋势相同,可是程度不同,V正它变大的趋势会小于V逆,变大的趋势后续达到一个新的平台,由于V逆它变大的程度大于V正,导致这个平衡会向着逆反应的方向。请大家注意,和浓度图像不同的地方就在于温度的改变会导致它有一个突变的过程,而不是像上面图当中有一个连接,这里是有一个等级式的上升。

将升高温度和降低温度放在一幅图当中,我们去观察,在正反应都是放热的情况下,升温或者是降温的图像是不一样的。对于正反应是放热的反应而言,升温平衡向着吸热反应方向移动,因为逆反应速率变大的程度会大于正反应速率变大的程度。而降温对于正反应是放热的反应而言,正和逆的速率都减小,但是正反应速率减小的程度要小于逆反应速率减小的程度,所以整个反应是向正方向移动的。
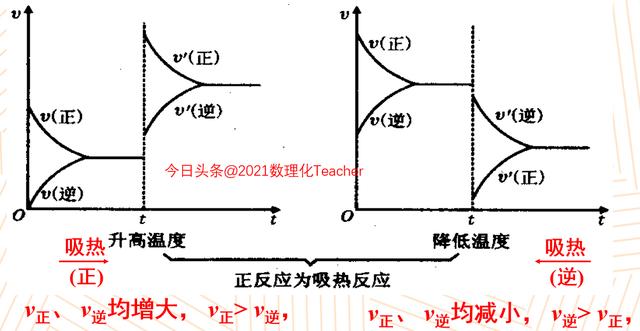
对于正反应是一个吸热的反应来说,升高温度的时候,反应向正方向进行,而降低温度的时候,平衡向着逆反应的方向移动。

第三个,我们来看一看压强对于速率和评分的影响。以氮气、氢气、合成氨这个反应为例,加压能够使正反应和逆反应速率都同时变大,但是由于加压气体向着体积方向减小的方向移动,所以正反应速率增大的程度要大于逆反应速率增大的程度,所以导致平衡正向运动。同理,减小压强的时候,气体平衡会向着气体体积增大的方向移动,减小压强、V正和V逆都会减小,但是程度不一样。和上面的温度图像有相似住处,加压的过程中依然会引起突变。

在这里我们要拓展一下,如果反应前后气体体积不变,那么加压的时候它会改变反应速率,可是不会影响平衡移动,但一旦增加压强,我们会关注到新反应的V正和V逆相等,但是他们会大于旧反应的V正和V逆,减小压强也是同样的道理。

最后我们要来看催化剂对速率和平衡的影响,使用正向的催化剂会使V正和V逆同等程度的增大,但是平衡依然不会发生移动,加入负催化剂原理是相同的。
以上就是今天的全部内容,如果有疑问可以留言,也欢迎大家积极转发。
,