原创Pan XX 抗菌科技圈

第一作者:Yin Gao, Zekun Wang
通讯作者:Dongdong Sun
通讯单位:安徽农业大学
研究速览
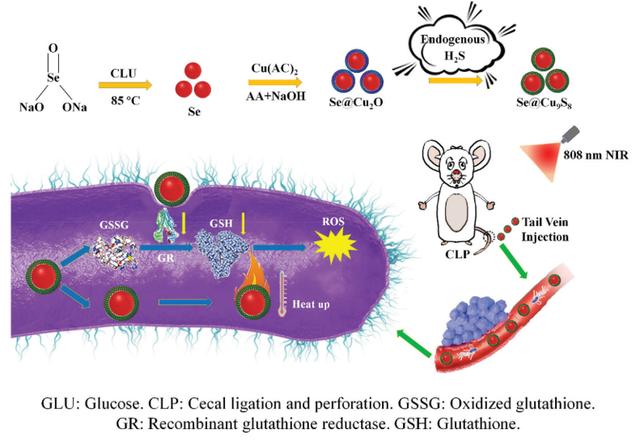
近期,安徽农业大学的孙冬冬课题组在Biomaterials Science 上发表了铜-硒纳米团簇的合理化设计及其光热及活性氧协同败血症治疗的研究工作。细菌感染引起的败血症的治疗仍然是一个巨大的临床挑战。由于败血症会在体内引起高水平的内源性H2S,研究人员可以通过原位硫化设计纳米药物来治疗败血症。在此,该工作设计了包覆Cu2O的非金属核壳硒纳米颗粒。利用ROS 治疗小鼠败血症。结果表明Se@Cu2O与内源H2S反应产生的光热效应的Se@Cu9S8纳米团簇具有协同抑菌作用。同时,Se@Cu2O具有副作用小、生物相容性高的特点。综上,研究结果验证了铜硒纳米团簇可能是一种通过内源性H2S的原位硫化、产生ROS和光热治疗治疗败血症的有效策略
要点分析
要点一:巧妙的材料设计,纳米硒可以在血液中自由移动,并将各种有效的纳米颗粒输送到人体的各个部位;同时,可以通过产生更多的活性氧来抑制大肠杆菌(E. coli)的感染;加之Cu2O与内源性H2S反应得到Cu9S8,然后合成的Cu9S8在808 nm NIR下可以产生热效应;
要点二:优良的抗菌活性,在近红外光下Se@Cu2O对革兰氏阴性大肠杆菌和革兰氏阳性金黄色葡萄球菌均显示很好的抗菌活性。其杀菌机理在于:Se@Cu2O NaHS在近红外作用下对细菌壁和细胞膜均有破坏作用,导致细胞内成分如核酸和K 的泄漏;同时,Se@Cu2O NaHS可以减少GSH的量从而导致ROS含量爆发从而杀死细菌。
图文导读

图1:(A)和(B) Se的SEM图像。(C)和(D) Se的TEM图像。Se@Cu2O由五种Se和Cu(AC)2的浓度比合成。(e) 1: 1。(F) 1.5: 1, (G / H) 2: 1, (I) 2.5: 1, (J) 3: 1。(K)和(L) Se@Cu2O的TEM图像。(M) Se@Cu2O的SEM图片。(N-P) EDS mapping图像Se@Cu2O。(Q) Se、(R) Cu2O和(S) Se@Cu2O的XRD谱图。(T)硒的XPS谱。(U) Se、Cu2O和Se@Cu2O的傅里叶红外光谱。(V) Se、Cu2O和Se@Cu2O的紫外-可见吸收光谱。(W) Se、Cu2O和Se@Cu2O的Zeta电位。(X) Se和Se@Cu2O的粒径分布。

图2: Se@Cu2O纳米颗粒的体外硫化过程。(A/E) Se@Cu2O NaHS在不同干扰条件下的紫外相对吸收光谱。(B/F) Se@Cu2O NaHS在不同pH条件下的紫外相对吸收光谱。(C/G) Se@Cu2O NaHS在不同浓度NaHS下的紫外相对吸收光谱。(D/H) Se@Cu2O NaHS在不同浓度Se@Cu2O下的紫外相对吸收光谱。通过5种NaHS与Se@Cu2O的浓度比。(i) 4: 1。(j) 4:2。(k / l) 4:3。(m) 4:4。(n) 4:5。(O/P) Se@Cu2O NaHS透射电镜图。(Q) Se@Cu2O NaHS扫描电镜下。(R T) Se@Cu2O NaHS元素分析图。

图3: (A/B/C/D)大肠杆菌和金黄色葡萄球菌存活率实验。(E)大肠杆菌和金黄色葡萄球菌经30 μgmL−1处理后的CFU图像。(F / G) CFU直方图。

图4: 细菌的完整性测试。(A)不同样品处理24小时后大肠杆菌和金黄色葡萄球菌的TEM图像。(B/C)用不同浓度的NaHS和30 μgmL-1 Se@Cu2O处理大肠杆菌24小时后培养基中核酸含量和K 含量。(D/E)不同浓度Se@Cu2O和40 μgmL-1 NaHS处理大肠杆菌24小时后培养液中核酸含量和K 含量。(F/G)不同浓度的NaHS和30 μgmL-1 Se@Cu2O处理金黄色葡萄球菌培养液24小时后的核酸含量和K 含量。(H/I)使用不同浓度的Se@Cu2O。40 μgmL-1 NaHS处理金黄色葡萄球菌24小时后培养液中的核酸含量和K 含量。

图5: Se@Cu2O NaHS在近红外光照下通过抑制谷胱甘肽还原酶(GR)活性增加ROS水平。(A)的大肠杆菌和金黄色葡萄球菌产生的ROS绿色荧光处理不同浓度Se@Cu2O 硫氢化钠2 h。Se@Cu2O 硫氢化钠在近红外光谱光治疗金黄色葡萄球菌和大肠杆菌(B) (C)。(D)大肠杆菌和金黄色葡萄球菌的谷胱甘肽水平不同浓度处理下Se@Cu2O 硫氢化钠的近红外光谱光2 h。(E / F)大肠杆菌和金黄色葡萄球菌的GR酶活性不同浓度处理下的Se@Cu9S8近红外光谱光2 h。

图6:体外光热成像。(A/B)热成像相机记录30 μgmL-1 Se@Cu2O与不同浓度的NaHS反应后,在808 nm近红外光下的热成像。(C/D)热像仪用40 μgmL-1 NaHS在808 nm近红外光下记录Se@Cu2O在不同浓度的热像。

图7:不同样品对小鼠创面愈合作用的代表性图片。

图8:(A/B)热成像相机记录不同浓度Se@Cu2O对小鼠创面的光热效应。(A/C)热成像摄像机记录不同浓度PAG对小鼠创面的光热效应。

图9:(A)小鼠败血症模型治疗示意图。(B/C)对照组和CLP小鼠血液中白细胞数量和中性粒细胞比例。(D)不同样品处理CLP小鼠血浆中H2S的水平。(E) CLP小鼠治疗后5天内各种标本的存活率。(F/G)不同样品处理CLP小鼠的MPO活性。
结论
这项研究展示了Se@Cu2O核壳纳米材料的制备以及将其作为抗菌剂用于败血症治疗的研究。结果显示,以治疗小鼠败血症。体外用NaHS模拟内源H2S和Se@Cu2O的硫化过程,在808 nm近红外光下表现出较强的抑菌活性。Se@Cu2O在近红外光作用下的体内抑菌机制主要表现为光热效应和ROS爆发。因此,我们在近红外光线下向尾静脉注射Se@Cu2O来治疗小鼠败血症。本设计的亮点在于巧妙地利用败血症小鼠体内高浓度内源H2S,在体内完成Se@Cu2O的原位硫化,不仅在近红外光下产生光热效应,还导致ROS爆发,协同抗菌治疗小鼠败血症。
全文链接:https://doi.org/10.1039/D2BM00172A
参考文献:Gao, Y.; Wang, Z.; Li, Y.; Yang, J.; Liao, Z.; Liu, J.; Guo, F.; Yang, E.; Wang, W.; Sun, D., A rational design of copper-selenium nanoclusters that cures sepsis by consuming endogenous H2S to trigger photothermal therapy and ROS burst. Biomater Sci 2022, 10 (12), 3137-3157.

投稿kangjunkejiquan@163.com
,