如何才能够正确地书写出化学反应方程式呢?这是每个初学者遇到的共同难题,也是每年化学中考的重点知识。中考试卷里与“方程式”有关的知识考题比较多,最简单的考题就是写出某一个化学反应的方程式;难度大一点的题目,比如“计算应用题”,这种题目的解答往往要根据反应的情况,先写出物质之间的反应方程式,再按要求计算出某一物质的质量。通过对各省中考化学试卷错题分析,发现这种类型的题目解答情况呈现两极分化现象,要么就是得到满分;要么就是一分未得。为什么有很多学生都会出现失分呢?其主要因为在于学生没有很好地掌握化学反应方程式的书写,从而导致相关计算题也无法得分。其实化学方程式的书写并不是很难,只要掌握“写、平、注、标、查”五个字,就可以正确地写出化学反应方程式。下面就对如何正确书写化学方程式进行详细阐述。
1、“写”-就是写出参加化学反应的反应物和生成物的化学式
要能够正确写出化学反应方程式,首先必须知道“什么是化学反应方程式”这一概念。“化学反应方程式”就是用化学式来表示化学反应的式子。言外之意,就是要想写出化学反应方程式,先要写得出来物质的化学式。所以建议大家在学习化学反应方程式书写时,先把化学式的知识好好复习一下,这是写方程式的基础。
其次,写化学方程式一定要遵循“两个原则”。
①遵循客观事实;以实验为依据;不能随意臆造世界上不存在的物质,也不能虚构根本就不可能发生的化学反应。
化学是一门以实验为基础的自然学科,每一种物质、每一个化学反应都比必须以实验事实为依据,我们不能够随意写出违背化学实验事实的物质和化学反应。如下图的化学反应方程式书写就不对,反应的生成物与实验事实不相符。

方程式中的物质化学式不正确,没有二氧化铁这种物质
下面化学反应式中铁的化学式不正确,铁是由原子直接构成的物质。氧气的化学式与氧气的组成不相符,氧气是由氧分子构成的,一个氧分子中有2个氧原子,而不是3个原子。

书写化学方程式时,化学式一定要正确
②必须遵循质量守恒定律,即参加反应的物质和生成的物质要保持元素的种类不能改变;原子的种类不变、原子的数目不变、原子的质量不变。如下图铁在氧气中燃烧的化学方程式两边的原子数目就不相等。

化学方程式左右两边的原子种类要相同,原子数目要相等
这两个原则是任何化学反应都遵循的物质变化规律,所以书写化学方程式的时候不能违背这两个原则,否则方程式就不正确。
2、“平”-就是配平化学方程式,让两边的原子种类和数目相等

配平化学方程式就是让方程式两边的原子种类和数目相同
书写化学方程式的第二步就是配平化学方程式,前篇已经讲到“化学反应的实质就是分子中的原子重新排列组合成新的分子”。换而言之,就是化学反应前后同种元素的原子种类和数目都保持不变;这也是配平化学方程式的依据,常见的配平化学方程式的方法主要有以下四种。
①观察法:是指通过眼睛观察两边的同种原子的数目是否相等。这种方法主要适合比较简单的化学反应方程式,而且化学方程式中的物质的化学式较简单的反应;对于复杂的化学方程式,就很难用该方法配平。

可以通过观察把左右两边的原子数目配平
像以上两个反应方程式就可以用观察法将其配平,比较方便省时。
②系数为“1”法:是指假设化学方程式中化学式组成相对较为“复杂”的化学式的计量系数为“1”,再根据这个化学式中的原子数目去配平其它化学式的计量系数。这种方法主要适合化学反应方程式中有一个较复杂的化学式的反应,例如配平下面方程式。

庚烷在空气中燃烧的化学方程式
配平方法:假设左边第一个化学式的系数为“1”,则左边碳原子数目一共是“7”个,氢原子数目为“16”;所以可以在右边二氧化碳的化学式前面加上“7”,水的化学式前面加上“8”;即二氧化碳的计量系数为“7”,水的系数就为“8”。再计算右边的氧原子数目(为22个),根据反应前后原子数目相等的原理,所以氧气前面的系数就为“8”,具体操作如下图所示。
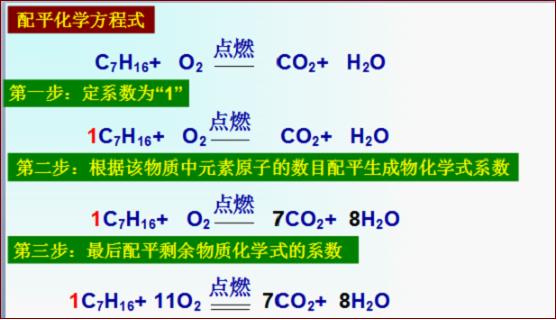
定化学式计量系数为“1”的配平方法
③奇数配偶法
一般选择“O”元素为配平对象,把“O”原子的系数为奇数的化学式前面配上数字,使其化学式中的“O”的数目为偶数。再根据这个已经配好的化学式的系数去配平其它化学式的系数,具体配平过程如下图所示。

奇配偶法就是奇数原子配成偶数原子
通过观察发现左边水中的O的数目为“1”,是奇数,所以我们可以在水前面加上数字“2”,让O原子数变为偶数。

再根据右边H的数目为“2”,去配平左边的H数目,则乙炔的计量系数就为“2”,即左右两边的H原子数目相对;再根据左边C的数目去配平右边二氧化碳的系数,即为“4”,最后根据左右两边氧原子数目也要相等,可以得出氧气的计量系数。

④最小公倍数法
最小公倍数法是配平化学方程式的常用方法,具体配平步骤如下:
第一步、先确定对象元素,一般选左右两边原子数目不同的元素为配平对象。
例如用最小公倍数法配平下面的化学方程式,可以选择氧元素为配平对象。

第二步、求出左右两边原子数目的最小公倍数。在上述化学反应中,左边氧原子的数目为“3”,右边氧原子的数目为“4”;则最小公倍数为“3X4=12”。
第三步、求出左右两边含有“对象元素”的化学式的计量系数。在上述化学反应中,左边四氧化三铁的计量系数对于最小公倍数除以四氧化三铁中氧原子的数目,即:12÷4=3;同理,氧化铝的计量系数为:12÷3=4。

第四步、再根据已经配平的原子数目,配平其它的原子数目。

根据左右两边铝原子数目相等,所以铝前面配上“8”;同理,生成物中铁的计量系数为“9”,这样反应物和生成物中各种原子的种类和数目都相等了。
3、“注”-就是注明该化学反应发生的条件。需要加热才能够发生的化学反应,其条件用“△”表示;在空气或氧气中燃烧的化学反应,其反应条件不能够写“燃烧”,应该写“点燃”;化学反应条件写在中间的的等号上面。
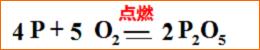
燃烧反应的条件为“点燃”,不是燃烧
4、“标”-就是标记出生成物的状态
①生成物中气体的标记方法。
如果反应物中没有气体参加,则生成物中的气体物质要在化学式的后面标记“↑”号,例如下面的化学反应方程式,生成的二氧化碳就要标记“↑”号,表示生成的是气体。

指标生成物的状态,不标反应物的状态
如果反应物中有气体参加,则生成物中的气体物质不标记“↑”号;

反应物有气体,生成物的气体不要标
②生成物中沉淀的标记方法,是针对在溶液中进行的反应。
如果反应物中没有固体参加,则生成物中的固体物质要在化学式的后面要标记“↓”号;如果反应物中也有固体参加,则生成物的固体物质的化学式后面不要注“↓”号。
5、“查”-就是检查化学方程式的正误,主要注意查看以下四点:
①一查:就是检查反应物和生成物的化学式是否正确,化学式中正负化合价的代数和一定要等于零;物质要符合实验客观事实,不能臆造任何物质。
②二查:就是检查化学方程式是否配平,即两边的元素种类是否相同;两边的原子种类和数目是否相等。
③三查:检查发生化学反应的条件是否符合化学实验事实。
④四查:检查生成物的状态是否标注的正确。
总之,书写化学方程式都要遵循质量守恒定律-即两边的原子种类和数目要相等。书写化学反应方程式也不是很难,对于初学者而言,只要掌握“写、平、注、标、查”,就可以避免在书写化学方程式的时候少走弯路,做到在中考中不失分。
,