转自《肿瘤瞭望》
乳腺癌是女性发病率第一位的恶性肿瘤,全世界每年新诊断乳腺癌患者约140万例,死亡50万人。2019年1月,国家癌症中心发布的最新的全国癌症统计数据显示,女性发病首位为乳腺癌,每年的发病约为30.4万,占女性全部恶性肿瘤发病的17.1%。且发病率以3%~4%的增长率急剧上升。随着医疗技术的不断进步,乳腺癌已成为临床上治疗方法最多、疗效最好的实体瘤之一。2019年中国临床肿瘤学会乳腺癌年会的数据显示,目前我国乳腺癌患者5年生存率已达83.2%,在过去10年间提高了7.3%。实践证明,对乳腺癌患者早发现、早诊断、中西医结合、规范治疗,可有效改善预后。建立乳腺癌分级诊治体系,完善乳腺癌筛查和早期诊断措施,重视患者治疗后康复,促其早日回归家庭和社会。

病例介绍
病例1基本情况:
患者,女性,43岁,个人史、既往史、肿瘤家族史均无特殊。
病史介绍:
患者因发现“左乳肿物7天”于2019.05.25在我院门诊行乳腺超声提示:左乳低回声结节:BI-RADS分级4b类;建议手术治疗。
手术治疗经过:
患者于2019.05.30行“左乳切除+腋窝淋巴结清扫术”。
术后石蜡病理示:
1、(左侧)乳腺浸润性导管癌(组织学分级:Ⅱ级),肿物大小1.5cm×1cm×1cm;
2、(左乳)乳头、皮肤及底切缘均未见癌;
3、(前哨)淋巴结(1/1)查见转移癌。
4、(左腋窝)淋巴结(0/13)未查见转移癌。
免疫组化:ER(2 ,70~80%),PR(2 ,40~50%),CerbB2(2 ),CK( ),E-cad( ),Ki-67( 5~10%),P63(-),P120( )。FISH检测:HER2基因未扩增。
术后诊断:左乳浸润性导管癌(T1N1M0 IIA期),“luminal B”型。
术后辅助治疗经过:
术后治疗方案:AC×4-T×4(密集方案) 放疗 内分泌治疗;具体用药:盐酸多柔比星脂质体注射液(多美素)40mg d1,环磷酰胺 0.9g d1,多西他赛 140mg d1,末次化疗时间2019.10.19。期间患者出现Ⅰ度胃肠道反应,Ⅲ度骨髓抑制。于2019.10.29开始行左侧胸壁及左侧锁骨区局部放疗1个疗程,期间同步应用OFS(戈舍瑞林) 他莫昔芬内分泌治疗,建议OFS(戈舍瑞林)满5年。
出院后随访:
1、应用醋酸戈舍瑞林3.6mg(q4w) 他莫昔芬10mg(bid)内分泌治疗满5年,期间注意定期行妇科彩超观察子宫内膜厚度;
2、定期门诊随诊、复查:自术后2年内,建议每3月复查一次;3-5年内,每6月复查一次;5年后,每年复查一次。复查内容包括:体格检查、胸部CT、腹部 腹膜后彩超、心脏彩超、颈部浅表及乳腺彩超及ECT等;
3、期间如有不适,及时就近医院或我院门诊就诊。
病例2基本情况:
患者,48岁,绝经前女性,个人史、既往史、肿瘤家族史均无特殊。
病史介绍:
患者于2019.04.26查体时发现右乳肿物,行乳腺超声提示:右侧乳腺11点可见一大小约1.5cm×1.0cm×1.3cm不规则低回声结节,分级4b级;建议手术治疗。
手术治疗经过:
患者于2019.04.30在当地医院行“右乳癌改良根治术”
术后石蜡病理示:
1、(右侧)乳腺浸润性导管癌Ⅰ级;肿瘤切面大小:2×1.2cm;
2、乳头及深切线无癌;腋窝淋巴结转移癌(2/16)。
3、免疫组化:ER(80%浸润癌细胞核强 )、PR(80%浸润癌细胞核强 )、HER2(10%浸润癌细胞膜呈不完整的弱染色,评分1 ,结果-),Ki-67(5%)。
后入住我科,会诊病理结果示:(右侧)乳腺浸润性导管癌(组织学分级:Ⅱ级),伴微乳头状分化,无明确脉管癌栓;乳头未见癌,(淋巴结)(2/17)查见转移癌。
免疫组化:癌细胞ER(3 ,>75%),PR(3 ,>75%),HER2(-),E-Cadherin( ),P120细胞膜( ),calponin(-),P63( ),Ki-67( ,>75%)。
术后诊断:右乳浸润性导管癌(T1N1M0 ⅡA期),“luminal B”型。
术后辅助治疗经过:
术后治疗方案:AC×4-T×4(密集方案) 放疗 内分泌治疗;具体用药:盐酸吡柔比星 80mg d1,环磷酰胺 1.0g d1,多西他赛 170mg d1,末次化疗时间2019.09.19。期间患者出现Ⅳ度胃肠道反应,Ⅲ度骨髓抑制。于2019.10.03开始行右侧胸壁及右侧锁骨区局部放疗1程,期间同步应用OFS(戈舍瑞林) 他莫昔芬方案内分泌治疗。
出院后随访:
1、继续应用醋酸戈舍瑞林3.6mg (q4w)2-3年,来曲唑片(2.5mg qd)内分泌治疗满5年,期间注意定期行骨密度测定;
2、定期门诊随诊、复查:自术后2年内,建议每3月复查一次;3-5年内,每6月复查一次;5年后,每年复查一次。复查内容包括:体格检查、胸部CT、腹部+腹膜后彩超、心脏彩超、颈部浅表及乳腺彩超及ECT等;
3、期间如有不适,及时就近医院或我院门诊就诊。
思考卵巢功能抑制推荐人群有哪些
《2016早期乳腺癌卵巢功能抑制临床应用专家共识》中,OFS的推荐使用人群是高危患者,中危患者考虑使用,低危患者不推荐使用。随着大宗的疗效和安全性数据出来以后,中国抗癌协会乳腺癌专业委员会修订了最新版(2018版)的共识 ,对中危患者及高危患者都进行了OFS的推荐,对低危患者推荐他莫昔芬单药治疗。这样就使得OFS的使用人群更明确,对于那些中危的患者中复发风险又相对比较低的人群,可以根据STEPP研究中的临床病理参数去计算患者的复发风险。对于那些复发风险稍微低一点的中危人群,我们可以考虑5年的TAM治疗,对于稍微高危的中危人群,我们还是建议加用OFS。
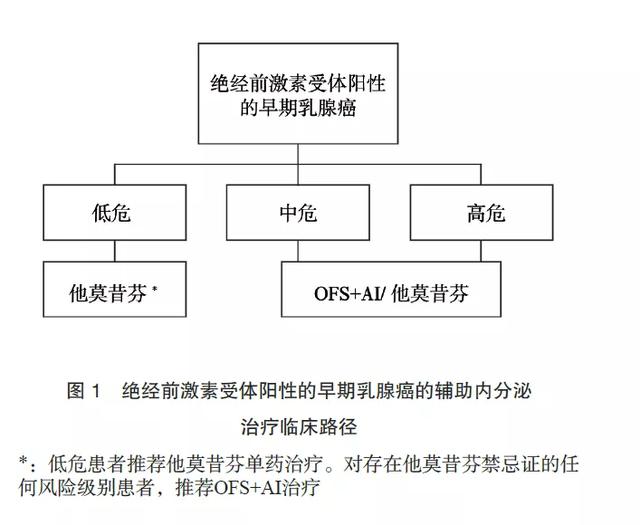

OFS的治疗疗程是2~3年还是5年?SOFT和TEXT研究中GnRHa的疗程为5 年,在SOFT研究中,5年OFS显著改善8年无病生存率和总生存率。ASTRRA研究中接受TAM 5年联合OFS 2年对比TAM 5年,显著改善5年无病生存率,绝对获益率为3.6%;显著改善总生存,减少69%的死亡风险。HOBOE-2研究中OFS的治疗时长同样为5年,结果显示OFS联合AI相较于联合他莫昔芬提高7.8%的DFS绝对获益。上述研究均证实了GnRHa良好的安全性和耐受性。所以对于临床高危的患者,如果患者能够耐受卵巢功能抑制,同时疾病复发风险又比较高,还是建议5年卵巢功能抑制治疗。但是具体到临床实践中,则有更多的需求,需要给患者更多的选择,就在今年的ASCO会议上公布的ASTRRA研究结果显示OFS TAM治疗2年的效果也不错。现在对于绝经前乳腺癌患者内分泌治疗的推荐,我们就有5个选择,分别是单药TAM治疗、OFS 5年 TAM 5年、OFS 2年 TAM 5年、OFS AI 2年及OFS AI 5年。我们临床医生有了更多的、更灵活的选择,比如临床实践中我们会遇到一些有生育需求的患者,或者那些中危偏低危的患者,OFS使用2年也是可以的。
《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》(2019版)推荐满足以下危险因素之一者:①G2 或 G3;②淋巴结阳性 1~3 个,③pT2 及以上推荐OFS+TAM 5年(1A);淋巴结 4个及以上阳性的患者推荐OFS+AI 5年(1A);《中国抗癌协会乳腺癌诊治指南与规范(2019版)》推荐的治疗时间是5年,但中危患者也可选择使用2~3年。2018年《中国早期乳腺癌卵巢功能抑制临床应用专家共识》建议GnRHa辅助内分泌治疗的疗程为5年,短于5年但超过2年的应用也有获益;2019年St.Gallen共识中给出的OFS最佳时长中,2~3年支持者占比24.5%,5年支持者占比55.1%,超半数支持OFS 5年疗程。
OFS方式的如何选择卵巢功能抑制的方式有放射去势、手术去势和药物去势,无论采取何种卵巢功能抑制手段,只要能把体内雌激素水平控制在要求范围内就可以。放疗去势现在基本不再使用,除了可能致癌外,亦不能保证所有患者的卵巢功能得到充分抑制。手术的优势是干净利落地进入绝经状态,不利之处是卵巢切除后,患者永不可能再回到绝经前状态。去势药物GnRHa能够抑制血清中雌激素水平,其抑制程度与手术去势相似。在激素受体阳性的转移性乳腺癌患者中开展的Intergroup研究显示,戈舍瑞林对乳腺癌治疗的客观有效率与手术去势相当,且使用戈舍瑞林患者安全性和耐受性良好。在辅助治疗的ZEBRA研究中,接受2年的戈舍瑞林辅助治疗后,77%的患者在3年内恢复卵巢功能,而接受CMF方案化疗的患者3年内仅有23%的患者卵巢恢复正常功能,因此使用GnRHa是绝经前乳腺癌患者一种优选的OFS方法,2016年的美国临床肿瘤协会(ASCO)关于OFS的指南更新也推荐使用GnRHa药物去势为OFS疗法的首选。总体而言,药物去势是非常有效的治疗手段。
参考文献:
《国家癌症中心:2019年全国癌症报告》
《中国早期乳腺癌卵巢功能抑制临床应用专家共识(2018版)》
《中国抗癌协会 乳腺癌诊治指南与规范(2019版)》
M C D O N A L D W A D E S 3 r d , H A C K N E Y M H ,KHATCHERESSIAN J, et al. Ovarian suppression in themanagement of premenopausal breast cancer:methods and efficacy in adjuvant and metastatic settings[J]. Oncology,2008, 75(3-4):192-202.
DEES E C, DAVIDSON N E. Ovarian ablationas adjuvant therapy for breast cancer[J]. Semin Oncol, 2001, 28(4):322-331.
JONAT W, KAUFMANN M, SAUERBREI W, et al. Goserelinversus cyclophosphamide, methotrexate, and fluorouracil as adjuvant therapy in premenopausal patients with node positive breast cancer:the Zoladex Early Breast Cancer Research Association Study[J]. J Clin Oncol, 2002, 20(24):4628-4635.
BURSTEIN H J, LACCHETTI C, ANDERSON H, et al.Adjuvant endocrine therapy for women with hormone receptor positive breast cancer:American Society of Clinical Oncology clinical practice guideline update on ovarian suppression [J].J Clin Oncol, 2016, 34(14):1689-1701.
专家简介

山长平
主任医师、教授
济宁医学院附属医院肿瘤科副主任、乳腺甲状腺肿瘤病区主任
中国抗癌协会会员
擅长常见、多发肿瘤的放疗、微创治疗及全身化疗等;尤其是乳腺癌、甲状腺癌的诊治及晚期肿瘤患者止痛方面
,