
一、分子式的确定:
确定有机物的分子式,与其燃烧的知识密切相关。有机物燃烧的通式为:烃:

烃的含氧衍生物:

1、实验式的基本求法:
实验式是表示化合物分子所含各元素的原子数目最简单整数比的式子。求化合物的实验式即是求化合物分子中各元素原子的数目(N)之比。
N(C):N(H):N(O)= m·ω(C)/12 :m·ω(H)/1 :m·ω(O)/16=a :b :c
其实验室为:CaHbOc
2、相对分子质量的基本求法:
有关化学量公式气体密度ρ(标况)Mr=22.4ρ相对密度d,另一已知气体的相对摩尔质量MMr=d·M物质的质量m,物质的量nMr=m/n
3、通式的运用:
熟练运用一些有机物的通式。烷烃为:CnH2n 2;烯烃为:CnH2n;炔烃为:CnH2n-2;苯的同系物为:CnH2n-6;饱和一元卤代烃为:CnH2n 1X;饱和一元醇为:CnH2n 1OH或者CnH2n 2O;饱和一元醛为:CnH2n 1CHO或者CnH2nO;饱和一元羧酸为:CnH2n 1COOH或者CnH2nO2。
二、结构式的确定
由于有机化合物中存在着同分异构现象,因此一个分子式可能代表两种或者两种以上具有不同结构的物质。
知道了某一物质的分子式,常常可以利用该物质的特殊性质,通过定性或者定量的实验来确定其结构式。
总而言之,确定有机物分子式和结构式的基本思路是:
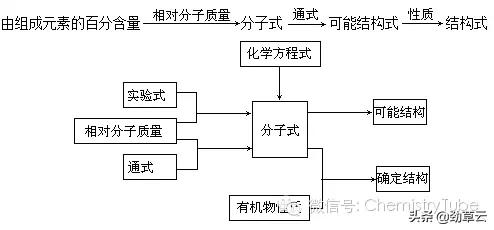
三、有关烃的混合物计算的几条规律
①若平均式量小于26,则一定有CH4
②平均分子组成中,l < n(C) < 2,则一定有CH4。
③平均分子组成中,2< n(H) < 4,则一定有C2H2。
最简式相同的有机物
(1)CH:C2H2、C4H4(乙烯基乙炔)、C6H6(苯、棱晶烷、盆烯)、C8H8(立方烷、苯乙烯)
(2)CH2:烯烃和环烯烃
(3)CH2O:甲醛、乙酸、甲酸甲酯、葡萄糖
(4)CnH2nO:饱和一元醛(或饱和一元酮)与二倍于其碳原子数的饱和一元羧酸或酯。如:乙醛(C2H4O)与丁酸及异构体(C4H8O2)
(5)炔烃(或二烯烃)与三倍于其碳原子数的苯及苯的同系物。如丙炔(C3H4)与丙苯(C9H12)
例1、某有机化合物中ω(C)=60%,ω(H)=13.33%,0.2mol该有机物质量为12g,则它的分子式为
A. CH4 B. C3H8O C. C2H4O2 D. CH2O解析:
解法一:先求12g有机物中含C、H的质量,确定还含O,再求实验式和相对分子质量,最后求分子式。
确定实验式为C3H8O
N(C):N(H):N(O)=m·ω(C)/12 :m·ω(H)/1 :m·ω(O)/16=60%/12 :13.33%/1 :26.67%/16=3:8:1确定分子式为(C3H8O)n
n =60/60=1 所以其分子式为C3H8O
解法二:先求相对分子质量然后求1mol有机物中含C、H、O的物质的量,确定分子式。
解法三:从选项入手去试C的质量分数满足60%的只有C3H8O。
答案:B
例2、某有机化合物A的相对分子质量(分子量)大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。请回答:(1)该化合物分子中含有几个氧原子,为什么?(2)该化合物的相对分子质量(分子量)是_________。(3)该化合物的化学式(分子式)是_________。(4)该化合物分子中最多含______个>C=O官能团。解析:
(1)设其中氧原子数为N,依据题意:
〔110×(1-52.24%)〕/16<N(O)<〔150×(1-52.24%)〕/16
3.3<N(O)<4.5
原子数目为整数,所以,该化合物分子中含有4个氧原子;
(2)Mr(A)=16×4/(1-52.24%)=134
(3)设分子式为CnHmO4,Mr(A)=134
用烃的部分除以14
134-16×4)/14=5,为CnH2n
易得其分子式为C5H10O4
(4)不考虑氧原子,饱和状态时为C5H10,而实际分子式比饱和状态时少了两个氢原子,说明只能形成一个不饱和键。在所给官能团>C=O中,恰好有一个碳氧双键,所以该化合物分子中最多含有一个>C=O官能团。
答案:(1)4;(2)134;(3)C5H10O4 ;(4)1。
例3、某烃A,相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢直接相连。已知有机物中含有—COOH基团时具有酸性。A在一定条件下氧化只生成G,G能使石蕊试液变红。已知:

试写出:
(1)A的分子式________________
(2)化合物A和G的结构简式:A______________、G________________解析:
该题主要考查:①烃的分子通式的应用和分子式的求法;②烃的基本碳架结构的判断;③应用信息和所学知识解决问题的能力。
(1)该烃分子中含有的碳原子数为

,含氢原子数为140-12×10=20。则该烃的分子式为C10H20。
(2)根据A在一定条件下氧化只生成G一种物质,可知A分子中双键两边应为对称结构;据G能使石蕊试液变红,可知双键碳原子上一定含有氢原子,据A分子中有两个碳原子不与氢直接相连可得出:
A的分子结构为:

;G的分子结构为

:答案:
(1)C10H20 (2)

、

例4、有机物A和B无论以何种比列混合,其组成的混合物中所含原子的核外电子总数不变,若A是分子中含8个氢原子的烃,B是分子中含3个碳原子烃的含氧衍生物,试回答下列问题:
(1)若相对分子质量之差为2,试写出两组符合上述条件的A、B的组合的分子式。
①A:_________B:_________ ②A: _________B:_________
(2)若相对分子质量相等,试写出一组符合条件的A、B的组合的分子式。
A:_________B:_________
解析:将化学问题抽象为数学问题,利用数学工具通过计算和推理解决化学问题,是近几年高考中考察学生能力的热点及难点问题。设:A的分子式为CxH8,则核外电子总数为6x 8,相对分子质量为12x 8;B的分子式为C3HyOz,则核外电子总数为18 y 8z ,相对分子质量为36 y 16z,据A、B核外电子总数相等有6x 8=18 y 8z,化简得:6x=10 y 8z ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅①(1)判断A、B相对分子质量的大小:因M(A)-M(B)=12x 8-(36 y 16z)=y-8;据B的分子组成C3HyOz可知:y≤8,则因M(A)-M(B)≤0,y-8= -2,y= 6;将y= 6代入到①得6x=16 8z,当:z=1时,x=4; z=2时,x=5.3(舍去);z=3时,x=6.6(舍去); z=4时,x=8,所以A为C4H8,B为C3H6O或A为C8H8,B为C3H6O4。(2)若y-8=0则y=8,将其代入①式得6x=8z 18,当:z=1时,x=4.3(舍去); z=2时,x=5.7(舍去);当z=3时,x=7符合题意, z=4,x=8.3(舍去)即A为C7H8,B为C3H8O3。答案:(1)①A为C4H8,B为C3H6O; ②A为C8H8,B为C3H6O4。(2)A为C7H8,B为C3H8O3。
A、B不论以何种比例混和,只要其物质的量之和不变,完全燃烧时生成的水的物质的量也不变,说明A、B中氢原子个数相同,所消耗的氧气也不变,则相差的碳原子应表示为(CO2)n的形式。答案:
A、B的分子式中氢原子数相同,且相差n个碳原子,同时相差2n个氧原子(n为正整数);C2H4O2;CH3COOH、HCOOCH3。
欢迎关注中学高分宝典
,




