
周末大餐……
翻译丨苏州市中医医院肛肠科 孙薛亮
审校丨南京中医药大学附属医院结直肠外科 杨柏霖
来源|医学界消化频道(CCCF—IBD学习驿站出品)
Management of complex perianal Crohn’s disease
Lara Aguilera-Castro, Carlos Ferre-Aracil, Ana Garcia-Garcia-de-Paredes, Enrique Rodriguez-de-Santiago,Antonio Lopez-Sanroman
Abstract: Patients with Crohn’s disease often develop perianal disease, successfully managed in most cases. However, its most aggressive form, complex perianal disease, is associated with high morbidity and a significant impairment in patients’ quality of life. The aim of this review is to provide an updated approach to this condition, reviewing aspects of its epidemiology, diagnosis and therapeutic alternatives. Emerging treatment options are also discussed. A multidisciplinary assessment of these patients with a coordinated medical and surgical approach is crucial.
Keywords Crohn’s disease, perianal disease, perianal fistula, perianal abscess
文献来源:Ann Gastroenterol 2017; 30 (1): 33-44
摘要
克罗恩病常并发肛周疾病,其多数可以被成功治愈。然而,最具有侵袭性的复杂性肛周克罗恩病并发症发生率高,显著降低患者生活质量。本综述通过回顾复杂性肛周克罗恩病的流行病学特征、诊断和治疗方法,更新对该病的认识。文中还讨论了一些新兴的治疗方法。内外科协同进行的多学科联合评估患者病情是极其重要的。
引言
克罗恩病(Crohn’s disease, CD)可能是一种由宿主与环境因素相互作用而产生的慢性炎症性疾病。近年来,CD的治疗有了显著的发展,例如生物制剂的问世、免疫抑制剂的合理使用、许多不良事件的有效预防、以及设计出更好的手术方法等等。然而,CD有时仍会给患者和临床医生带来意想不到的问题,严重影响个人生活质量。肛周克罗恩病(perianal Crohn’s disease, PCD)是最具代表性的侵袭性病变之一。受影响的患者不仅遭受短期病变的痛苦,其生活质量也会降低;长此以往,社会活动也可能会受到负面影响。
本文力图提供关于复杂性肛周克罗恩病(complex perianal Crohn’s disease, CPCD)现有观念的概述。肛瘘是CPCD最具特征性表现,我们予以重点讨论以更好地了解这种特殊的CD临床特征。
CPCD的定义、流行病学及医疗负担
尽管有多种新兴的、疗效较好的内科治疗方法,但许多CD患者依然存在相当多的临床症状[1]。当CD影响肛周区域时,其主要表现形式为肛瘘和肛周脓肿。PCD的发病率占CD患者的21%-54%。结肠受累的患者发病率高,达41%;与之相比,病变局限于回肠的患者发病率仅为12%。PCD被确认为预后差的指标,并与医疗成本的增加相关[2-3]。
PCD是一类没有共性的疾病。一些病例可以通过简单的内、外科治疗处理,同时不影响疾病的整体医疗负担。然而,一些病例则需要更加激进的方法来控制疾病。CPCD没有明确的定义,甚至在最新的欧洲克罗恩病和结肠炎组织(European Crohn’s and Colitis Organization, ECCO)的CD临床诊治指南中也没有相关定义[3]。本文根据Sandborn[4]提出的标准将CPCD定义为:高位复杂性肛瘘(累及超过2/3外括约肌的高位肛瘘,包括高位括约肌间肛瘘、高位经括约肌肛瘘、括约肌外侧肛瘘或括约肌上肛瘘),有多个外口,或伴发肛周脓肿、直肠阴道瘘、肛管直肠狭窄及内镜下活动性直肠炎。
复杂性肛瘘比简单瘘管更难治疗。St Mark’s 医院在生物治疗出现以前(1994年)的研究显示,治疗的不连续性导致高复发率[5]。这项研究中,87例瘘管型CD患者从发病起随访6年,65%的患者仍然存在肛瘘,其中80%为复杂性肛瘘。随访期间,14%的患者瘘管始终没能愈合,50%的复杂性肛瘘患者最终需要进行造口或肠道切除。肛瘘或直肠阴道瘘中位愈合时间2.6年。荷兰鹿特丹Erasmus医学中心的Molendijk等通过大样本的回顾性队列研究评估CPCD的自然进程(主要在生物治疗前时代,1980年至2000年)[6]。232例患者,中位随访10年,78%的PCD患者在某个时间段会发展为复杂性肛瘘。与复杂性肛瘘相比,简单肛瘘治愈率更高(88.2% vs. 64.6%),复杂性肛瘘复发率更高(41.9% vs. 26.7%)。至于手术结果,复杂性肛瘘患者更可能接受永久性粪便改道(63.8% vs. 26.7%)和直肠切除(25.5% vs. 6.7%)。作者认为,传统治疗方法仅有1/3的CPCD患者在长期随访获得持久缓解。
必须强调的是,CPCD会花费更多的医疗资源,造成沉重的经济负担。一项近期的西班牙多中心、回顾性研究,依据临床特点和治疗方法分析了西班牙马德里地区97例CPCD患者临床实践中所需要的社会现实负担[2]。抗生素、免疫抑制剂、生物制剂和手术治疗分别占32.3%、20.5%、20.3%和27%。每个患者平均年花费8289欧元,其中75%为药费(主要是生物制剂费用),12.4%为住院和手术费用,7.7%为门诊随诊费用。之前的一项研究显示,在同一地区CD直接医疗费用为每位患者年平均花费2104-4464欧元(如果采用生物制剂,则高达10594欧元)[7]。因此,作者认为较少的一部分CD患者(主要是合并肛瘘的CPCD患者)消耗了大部分与疾病相关的医疗资源和经济负担。此外,这种类型的研究很少考虑到由于疾病导致的无法工作或病假形成的间接费用,然而,这些也应该包含在CPCD的总体医疗负担中。
PCD和CPCD在年轻患者中发病率高。大约25%的CD患者在儿童期或青春期出现症状。据估计1/3儿童患者将会形成肛周病变。Zwintscher等进行了一项关于PCD对年轻患者影响的回顾性研究[8]。他们研究了一组诊断为儿童炎症性肠病的患者, CD占其中63%。4.1%的患者出现PCD,其中19.17%为复杂性肛瘘。伴有肛周疾病的儿童患者可能需要进行2次手术。另外,与没有PCD的住院患者相比,他们平均住院日多1.3天,多花费5838美元。
正如上文所述,由于对内科治疗不敏感,CPCD患者通常需要手术治疗。但目前关于肛周瘘管型CD术后生活质量评估的研究罕见报道。Riss等在维也纳进行了一项评估PCD患者生活质量和性功能的研究[9]。他们随访了88例手术治疗PCD的患者(排除先前造口的患者)。患者完成了包含勃起功能国际指数(IIEF)、女性性功能指数(FSFI)、健康调查12条简表(SF-12)和炎症性肠病生存质量问卷(IBDQ)在内的自填式问卷调查表。根据年龄和性别将患者与健康对照组进行匹配。结果显示,与健康对照组相比,健康调查12条简表(包括生理和心理健康)和炎症性肠病生存质量问卷评分较低的患者生活质量降低。然而,令人惊奇的是两组性功能问卷调查结果无显著差异。
结论:CPCD在CD患者中并不罕见,发病率较高,显著降低成人和儿童患者的生活质量,花费更多的医疗成本。
CPCD分型和诊断
典型的肛瘘症状是排便时肛门疼痛、肛周瘙痒、出血和溢脓。脓肿引流术后通常形成肛瘘。瘘管型PCD的鉴别诊断包括:外伤、化脓性汗腺炎、结核、HIV感染、性病淋巴肉芽肿、肛周放线菌病和直肠后皮样囊肿等。另一方面,肛周脓肿也可以表现为肛周疼痛,严重者可伴有发热。体格检查发现肛周肿胀、红斑、硬结和波动感时,应怀疑存在肛周脓肿。但是,有时上述典型症状很少出现,因而单纯体格检查不足以排除肛周脓肿。
克罗恩病肛瘘的分型对制定最佳治疗方案起重要作用。在现行的诸多分类方法中,Park’s分类是最符合解剖特征的。它描述了5种不同类型的瘘管:皮下瘘、括约肌间肛瘘、经括约肌肛瘘、括约肌上肛瘘和括约肌外肛瘘[10]。美国胃肠病协会制定了一种简单的分类方法,将瘘管分为简单和复杂两种[4]。简单肛瘘是累及皮下组织的低位瘘管,包括皮下瘘、位于齿线下方的括约肌间瘘和经括约肌瘘,并且只有单一内、外口,无肛周并发症。相反,复杂性肛瘘,如高位括约肌间肛瘘、高位经括约肌肛瘘、括约肌上肛瘘和括约肌外肛瘘,有多个内、外口,伴发脓肿、直肠炎、直肠狭窄、直肠膀胱瘘或直肠阴道瘘。由于潜在的生殖器并发症,女性前侧所有类型的肛瘘通常视为是复杂性肛瘘。
影像学检查在评估瘘管解剖学特征、排除脓肿等感染性疾病、制定治疗方案和监测治疗反应至关重要。复杂性肛瘘均应进行盆腔核磁共振检查(magnetic resonance imaging, MRI)(图1)。MRI在鉴别诊断肉芽组织和纤维化组织,诊断瘘管型脓肿具有高准确性,且无创伤、无辐射。MRI诊断特异性在76%-100%之间[11]。机器设备不普及和检查费用高限制了MRI广泛应用。
经肛直肠腔内超声(endoanal ultrasound, EUS)在诊断肛瘘方面可作为MRI的可靠替代检查。EUS可以获得2D或3D图像,并可通过局部注射双氧水提高可视性[12]。其限制性在于过多依赖操作医师的经验,直肠狭窄的患者无法检查,以及显示较远区域(如坐骨直肠窝)准确性较低。一些学者认为高分辨率3D EUS能显示所谓的“克罗恩病超声瘘管征”,其特征是低回声的瘘管被边界清晰、边缘为窄低回声带的高回声区包绕。这个特征可以区分CD瘘管与其它类型瘘管[13],但这未经对照研究证实。
一项Meta分析对照研究了MRI与EUS对肛瘘评估价值,共纳入4项研究,结果发现MRI(0.87, 95%置信区间(confidence interval, CI)0.63-0.96)与EUS(0.87, 95%CI 0.70-0.95)敏感性一致,但MRI(0.69, 95%CI 0.51-0.82)特异性高于EUS(0.43, 95%CI 0.21-0.69)[14](表1)。经会阴超声检查是另一种检查CD肛周并发症的方法。几项研究报道了其诊断肛瘘和直肠阴道瘘的敏感性高达85%[15]。
由经验丰富的结直肠外科医生在麻醉下检查(examination under anesthesia, EUA)是被ECCO指南推荐的金标准,肛周疾病诊断准确度达90%[16]。EUA同时可完成治疗措施,如脓肿引流术、挂线术或肛瘘切开术。如果疑诊脓肿,EUA应即刻进行(图2)。
一些研究已经对比分析了MRI、EUS和EUA诊断CPCD的适宜性。一项纳入32例患者的前瞻性研究显示三者的准确度分别为87%、91%和91%[16]。EUA联合MRI或EUS可使其准确度提高到100%[16]。另一项研究发现MRI(0.97, 95%CI 0.92-1.01)在鉴别诊断复杂性病变与简单病变的敏感性高于临床检查(0.75, 95%CI 0.65-0.86),与EUS相似(0.92, 95%CI 0.85-0.99)[17]。
不推荐瘘管造影和CT用于CPCD的诊断和分型。它们受限于电离辐射,且区分瘘管与盆底肌肉分辨率差[18]。此外,瘘管造影还存在并发症。
所有CPCD患者均需完善直肠乙状结肠镜检查,明确炎症的范围和严重程度,排除狭窄、恶性肿瘤等并发症[18]。持续存在的直肠炎被认为与瘘管不愈合和直肠切除率高相关[5]。
多种不同的方法和指数被用于临床评估肛瘘活动度。肛周疾病活动指数(perianal disease activity index, PDAI)评分包含5个要素:瘘管分泌物、疼痛和活动受限、性生活受限、肛周疾病类型、硬结程度(表2)[19]。PDAI大于4分提示活动性瘘管或存在局限性炎症,准确度达87%[20]。多个临床试验证实了这一评分系统[21]。依靠检查者观察的所谓“瘘管分泌物评估”是一种简单评估瘘管活动度的方法。手指加压后可观察到脓液溢出的瘘管为肛瘘活动。在连续两个观察期内,有分泌物溢出的瘘管数量减少50%以上,则认为临床改善或应答;不存在分泌物溢出的瘘管则确认为缓解。
瘘管仍存在炎性改变时,外口有时会愈合。因此,推荐应用MRI或EUS监测内、外科治疗后CPCD的变化。2003年van Assche提出了MRI评分,虽被临床证实,但与PDAI相关性差[22]。
CPCD的治疗
在接触PCD患者之前必须强调以下几点:
a)PCD是常见病,其症状轻微与解剖侵袭性不相符。因此,在第一次接触疑似或已确诊的CD患者时,必须进行全面的临床检查,且需间断性进行重复检查,尤其当新的症状出现时。
b)PCD的诊断首先需遵循直接损伤控制原则。这其中包含局部感染的治疗,因为它是引起患者不适和肛门括约肌损伤的重要因素。通常采用环丙沙星联合甲硝唑抗感染治疗。当感染是主要原因时(盆腔脓肿),可采用阿莫西林克拉维酸钾、注射用亚胺培南或哌拉西林他唑巴坦抗感染治疗。
c)如果存在肛周脓肿,引流是控制局部感染的基本方法。
d)类固醇激素治疗PCD无效,应避免使用。
e)必须制定治疗计划。所有患者的诊疗计划均需包含外科会诊。
f)作为诊疗计划的一部分,完善的辅助检查也是必需的。可依据本地区推荐的指南完善硫嘌呤甲基转移酶、血清乙型或丙型肝炎病毒和潜伏期结核等检测。
手术
尽管这是一篇胃肠病学综述,但需要强调的是没有外科会诊的CPCD诊治过程永远是不完善的。对于比较幸运的患者来说,外科医生只能袖手旁观。更多情况下,需要外科手术来控制疾病的发展。也许更重要的是,手术是治疗顽固性CPCD患者的最后唯一方法。
一般来说,外科医生首次参与治疗CPCD是进行脓肿引流。在脓肿早期,手术应采用相对保守的方法,以防止损伤肌肉组织,保护肛门功能。脓腔内置管可充分引流。在这一阶段,应避免挂线引流。在脓肿已经充分引流,影像学和内镜检查显示肛瘘轮廓形成后再挂线引流会更加安全。需要强调的是,没有适当的外科手术协同的内科治疗成功率较低,有时甚至是冒险的。
挂线和拆线的准确时机仍是持续争论的问题。事实上,ECCO指南没有明确提出时间间隔。正如上文所述,在急诊手术有时应避免挂线。局部脓毒血症得到有效控制,影像学和内镜检查显示肛瘘的解剖轮廓,再由经验丰富的外科医生完成挂线会更加安全[23]。挂线可根据需要保留足够长的时间,甚至几个月。在术后外科随访期间,根据个人情况决定拆线时机。Joline de Groof等最近报道了一篇关于挂线治疗的系统性回顾分析,共纳入10项非对照研究,包括305例引流挂线治疗的患者[24]。瘘管完全闭合率为13.6-100%,复发率为0-83%。外科医生决定引流挂线拆除时间,通常在3周至40个月不等。一些近期研究表明在抗肿瘤坏死因子(tumor necrosis factor, TNF)α治疗缓解后,或英夫利昔单抗治疗至少5次后拆线复发率较低[25]。挂线联合免疫抑制剂或抗TNF-α可比单纯挂线取得更佳疗效[24]。
尽管需要影像学检查辅助,但EUA仍然是确定瘘管位置和解剖关系的金标准[16]。经验丰富的外科医生的作用不容小觑。肛周解剖并不简单,应严格按照诊疗需求行事,避免超范围。在一些病例中,肛周病变相当复杂,组织破坏严重,以致临时性回肠造口是控制组织损伤,减轻病情的最佳选择[26]。造口可促进损伤组织愈合,后期可通过造口回纳完成肠道结构重建。
在内科治疗期间症状不缓解或出现新症状时,有时需进行二次EUA。如果治疗方案需要大调整,如从免疫抑制剂转换到生物制剂或使用激进的疗法,则再次行EUA是非常重要的。
药物难治性病例需要手术治疗,但这显然超出了本综述范围,读者可参考近期综述性文献[27]。经验丰富的外科团队可尝试进行推移皮瓣或粘膜瓣、激光治疗术、瘘管结扎术等保留括约肌手术。
永久性回、结肠造口有时是唯一选择[26,28]。直肠切除术需根据每个患者的情况慎重考虑。当直肠炎持续存在(有时表现为造口周围脓皮病)、恶变可能、直肠残端而导致瘘管始终不愈合时,可考虑行直肠切除术。但必须记住可能会导致如男性勃起功能障碍、形成会阴部窦道等手术并发症[29]。
抗生素
如前文所述,抗生素被推荐用于治疗克罗恩病肛瘘,而不仅仅用于控制肛周脓肿。抗生素的用药指征存在差异,且目前尚不清楚抗生素治疗是否能够作为治疗复杂瘘管的独立替代疗法[30]。我们的观点是永远不要单独使用抗生素。ECCO指南推荐抗生素联合硫唑嘌呤或巯嘌呤可作为复杂瘘管的一线治疗方案[3]。抗生素可有效改善症状,但不能诱导瘘管完全愈合。
甲硝唑和环丙沙星是推荐用药。常用剂量是甲硝唑20mg/kg/d或750-1000mg/d分3或4次口服;环丙沙星1000-1500mg/d分2次口服。关于治疗期限没有建议,但大部分研究持续8-12周。两种药物也可联合使用。
尽管单用抗生素治疗PCD是被推荐的,但其推荐依据仅是非对照的病例队列研究,以及一项短期高质量研究。后者是一项随机、双盲、安慰剂对照试验,比较了25例患者采用环丙沙星、甲硝唑和安慰剂治疗10周的疗效[31](表3)。接受环丙沙星治疗的患者获得更多的缓解和应答,但差异不显著。
抗生素联合免疫抑制剂或生物制剂的疗效也有报道。一项前瞻性、开放试验显示,抗生素(甲硝唑或环丙沙星)联合硫唑嘌呤治疗20周时获得应答高于单用抗生素[32]。一项纳入24例患者的双盲、安慰剂对照研究显示环丙沙星联合英夫利息单抗(infliximab, IFX)疗效优于单用IFX[33]。一项纳入76例患者的随机、双盲、安慰剂对照试验显示,阿达木单抗(adalimumab, ADA)联合环丙沙星治疗组71%的患者获得临床应答,而ADA联合安慰剂治疗应答率为47%(P=0.047)。然而,两组在治疗24周时临床应答无差异[34]。
一项纳入74例患者的设盲、随机、安慰剂对照研究比较了外用10%甲硝唑软膏与安慰剂在4周内疗效。甲硝唑软膏未降低PDAI评分,但可显著减少肛周分泌物[35]。
免疫抑制剂
巯基嘌呤类药物
目前还没有随机对照试验来评价巯基嘌呤类药物治疗复杂性肛瘘疗效。现有数据主要来自一些队列研究和一个纳入5项随机、安慰剂对照试验的Meta分析结果(肛瘘闭合作为第二终点指标)。在这些研究中,巯基嘌呤类药物(硫唑嘌呤2-3mg/kg和6-巯基嘌呤1.5mg/kg)似乎对诱导肛瘘缓解有效(风险比4.44,95%CI 1.5-13.20)[36](表4)。即使巯基嘌呤类药物有效,起效时间也需要数周,甚至数月。因此,一些研究评价了巯基嘌呤类药物在与抗生素或抗TNF制剂联合使用中发挥的作用。一项前瞻性试验评价了硫唑嘌呤在抗生素(环丙沙星或甲硝唑)治疗8周后维持应答的作用,结果发现在抗生素撤销后使用硫唑嘌呤维持治疗获得更高的应答率(48% vs. 15%, P=0.03)[32]。关于巯基嘌呤类药物联合IFX治疗的研究表明其有助于改善应答。虽然缺少对照研究,但ECCO指南仍推荐抗生素联合手术引流、巯基嘌呤类药物维持治疗是治疗CPCD的一线治疗方案[3]。巯基嘌呤类药物或许应该和抗TNF联合使用来促进并维持应答。
钙调磷酸酶抑制剂
一项小样本安慰剂对照试验显示,他克莫司(0.2mg/kg/d)可有效改善症状(43% vs. 8%, P<0.05),但无法使瘘管完全闭合[37]。最近的一项研究评价了他克莫司治疗对抗TNF不耐受或无应答的重症CD的疗效[38]。该研究纳入了15例合并肛瘘患者,其中5例可观察到少量分泌物。他克莫司血药浓度10-15ng/mL时治疗效果最好,能够避免或推迟手术。对于抗TNF治疗无应答的患者,他克莫司可作为考虑手术之前的拯救性治疗。
一项回顾性研究显示,4/13患者在静脉注射环孢素后再口服环孢素瘘管完全闭合,但停药后肛瘘复发[39]。由于数据有限,环孢素治疗CPCD的证据尚不明确。
其他免疫抑制剂
多项小样本病例队列研究表明甲氨蝶呤治疗瘘管型CD有效[40]。然而,没有甲氨蝶呤专门针对CPCD治疗的研究,因此目前不是推荐用药。
由于沙利度胺可以抑制TNF-α、γ-干扰素和白细胞介素(interleukin, IL)-12等,因此它被作为拯救性治疗用药。多项非对照研究已经评价了其治疗难治性CD的疗效,其中部分患者合并肛瘘。Yang等在2015年发表一篇关于沙利度胺治疗IBD疗效的综述[41]。在纳入的4项病例系列研究,共40例采用沙利度胺(50-300mg/d)作为诱导治疗的PCD患者。10例获得完全缓解,11例获得部分应答,5例无应答,剩余14例因副作用停药。多项个案报道和病例系列研究报道了一些麦考酚酸脂治疗CD的益处。但是麦考酚酸脂和沙利度胺都不是推荐的标准临床用药。
生物治疗
抗TNF制剂
抗TNF制剂治疗CPCD的现有证据级别最高。然而,仍有一些应用方面的问题需要进一步探讨,如是否需要合用抗生素、免疫抑制剂或挂线引流。虽然ECCO指南推荐抗TNF制剂作为对巯基嘌呤和抗生素药物耐受患者诱导和维持治疗的二线用药,但大部分专家主张应用“降阶梯”治疗,即将抗TNF制剂作为CPCD患者诱导治疗的首选用药[18]。诱导缓解期可以联合使用抗生素,而维持治疗期则联合使用巯基嘌呤类药物至少1年。文献报道大约11%患者在抗TNF制剂治疗期间发生肛周脓肿[42](表5)。因此,在应用抗TNF制剂前进行肛周脓肿引流非常重要,可以有效避免感染发生并优化疗效。
在一项设计以强调瘘管闭合为终点指标的随机对照研究证实IFX是唯一可以有效诱导复杂性肛瘘闭合的药物。这项研究中,5或10mg/kg的IFX在0、2、6周治疗后应答率为62%,安慰剂组仅为26%。5mg/kg剂量组中55%的患者瘘管完全闭合,安慰剂组为13%[42]。另一项随机、安慰剂对照研究评估IFX诱导治疗有应答的瘘管患者应用IFX维持治疗的作用(5mg/kg/8周,维持1年)。54周时36%患者瘘管分泌物完全消失,安慰剂组为19%(P=0.009)[43]。其它一些非对照研究报道也显示IFX具有满意的诱导和维持效果,13-90%的患者瘘管分泌物完全消失[44]。IFX维持治疗可显著减少住院时间和手术次数,因此应该常规应用[45]。正如上文讨论,抗生素可以作为抗TNF制剂的辅助治疗。虽然IFX提供了最好的临床疗效,但临床缓解与影像结果显示瘘管持续活动相矛盾。MRI或超声研究显示仅有少数瘘管愈合,而多数管道持续存在。一项研究报道显示,尽管54%患者获得临床应答并瘘管分泌物消失,但超声检查仅有18%的患者瘘管处于静止期[46]。这可能是复杂肛瘘患者在临床缓解1年后停止治疗高复发率的主要原因。因此,建议延长治疗周期,并在考虑停止治疗前应用影像检查评估瘘管情况。有趣的是,2016年消化病周的一项研究表明瘘管愈合所需的IFX血药浓度高于粘膜愈合[47]。
3项将瘘管完全闭合或改善作为第二终点指标的随机对照试验对比研究了阿达木单抗(ADA)与安慰剂疗效。最近一项研究纳入117例主动引流的肛瘘患者,在ADA诱导治疗后随机接受ADA或安慰剂维持治疗1年,结果显示56周时ADA组瘘管缓解率更高(33% vs. 13%, P<0.02)[48]。
虽然没有针对设计的随机、安慰剂对照研究来证实聚乙二醇化赛妥珠单抗治疗肛周疾病疗效,但其疗效作为第二终点指标已被报道。一项试验对比研究了赛妥珠单抗诱导应答后采用赛妥珠单抗和安慰剂维持治疗的疗效,结果发现治疗组36%患者肛瘘完全闭合,而安慰剂组为17%(P=0.038)[49]。
其他生物治疗
关于维多珠单抗治疗肛周疾病疗效的数据有限,且结果不明确。一项随机对照研究评估了维多珠单抗治疗CD的疗效,结果发现维多珠单抗组8周引流瘘管闭合率显著高于安慰剂组(41.2% vs. 11%, P=0.03)[50]。
优特克单抗是一种抗IL-12/IL-23单克隆抗体,其在Ⅱb期和Ⅲ期临床试验中显示治疗CD有效。不幸的是,这些研究没有显示其治疗PCD的作用[51]。迄今为止,最详实的数据来自一项近期发表的观察性研究。2016年Wils等完成了一项多中心、回顾性分析研究,纳入12例PCD患者,8例临床症状改善,其评判依据为医生的整体评估、避免长期使用糖皮质激素或手术治疗、以及没有应用其他免疫抑制剂[52]。
其它治疗方法
近几十年来,一些新方法的出现有望为标准治疗无应答的患者提供替代疗法。然而,它们在治疗方法中的地位及其临床实用性有待进一步观察,因为大部分现有数据来自具有高偏倚风险的研究。
高压氧治疗(hyperbaric oxygen therapy, HOT)
HOT是在增加的大气压下呼吸100%的氧气。它导致血氧分压增加,进而提高缺氧肠组织和未愈合肛瘘的氧合。此外,据报道HOT具有免疫调节特性,可降低IL-1、IL-2和TNF-α水平,上调缺氧耐受的分子通路(缺氧诱导因子-1,血红素加氧酶-1)[54]。
2014年Dulai等系统评价了HOT治疗IBD的疗效和安全性[55]。他们整合了17项不同研究的数据,其中多数是个案报道,仅有一项为随机临床试验。纳入病例中包含40例PCD患者,开始治疗前中位病程为2年, 21例患者伴有肛瘘(复杂瘘管为主)。大多数患者对5氨基水杨酸、糖皮质激素和免疫抑制剂治疗应答差。HOT治疗总应答率为88%(18/40完全治愈,17/40部分治愈),但有2例患者因副作用放弃治疗。然而,必须强调的是,纳入的研究在治疗应答评估、症状评估、随访次数和时间方面具有很大的差异性。
HOT的不良反应并不常见(0.01%)。似乎IBD患者对HOT耐受性较之其他适应症更强,如放射性直肠炎(0.2%)。耳膜穿孔和心理不耐受(幽闭恐惧症)是最常见的副作用。气胸、近视、肠穿孔和癫痫也有报道[55]。
在本系统性回顾研究完成之前,没有进一步的相关研究出现。
间充质干细胞(mesenchymal stem cells, MSCs)
MSCs是具有强效抗炎、免疫调节和成纤维细胞样愈合特性的非造血干细胞。目前,从脂肪或骨髓中采集的异体或自体MSCs已经用于治疗PCD[56]。来自多个Ⅱ期临床试验的数据证实这种治疗方法是安全的,并且对一些患者可能有用。这些研究纳入的研究主体差异性大,大部分是对巯基嘌呤类和抗TNF药物不应答,瘘管闭合率在37-85%之间。最常见的给药途径是病灶局部注射,仅有一项研究使用静脉途径[56]。2015年Ciccocioppo等报道了10例患者超过7年的前瞻性研究结果。1年期瘘管无复发率为88%,2年期为50%,37%患者无不良反应。这些结果支持该疗法的有效性和长期安全性[57]。最近,一项随机对照的Ⅲ期临床试验显示MSCs对传统或生物治疗失败的患者疗效良好[58]。这项研究纳入的212例患者随机接受病灶注射异体脂肪干细胞或生理盐水(安慰剂),24周时干细胞组肛瘘缓解率更高(50% vs. 34%, P=0.024)。虽然MSCs疗法看起来前途光明,但仍有一些关键问题需要解答,例如理想的MSCs类型、所需细胞剂量、注射次数及其远期疗效。
纤维蛋白胶注射
纤维蛋白胶注射是一项极具吸引力、操作简单的技术,其通过激活凝血酶原形成纤维蛋白凝块,机械性填封瘘管。纤维蛋白凝块逐渐发生纤维蛋白溶解,同时激活组织愈合机制,进而永久性闭合瘘管。非对照研究报道了令人鼓舞的结果,成功率为60-85%[59]。最具相关性的研究发表在2010年,Grimaud等进行了一项多中心、开放式、随机对照研究,纳入77例患者。纳入患者的CDAI评分≤250,引流时间超过2个月的肛门(或低位直肠)与会阴、外阴或阴道之间的瘘管[60]。在第8周,纤维蛋白胶组临床缓解率为38%,对照组为16%;复杂性肛瘘的亚组疗效差。作者重新评论CDAI评分低的患者,推测纤维蛋白胶是一种纯粹的机械治疗,只有在炎症控制后才能进行。
肛瘘栓
目前有Surgisis®和GORE BioA®两种肛瘘栓,其中应用最广的是Surgisis®。它是由冻干猪小肠黏膜下层组织制成的生物可吸收栓。GORE BioA®栓是由可吸收合成化合物制成,外形设计成圆锥形,一端融合在便易于固定于瘘管内口的平盘上。最近,一项纳入8项非随机、前瞻性试验和4项回顾性队列试验的系统性回顾研究,共84例患者,平均年龄45岁,中位随访时间9个月。Surgisis®和GORE BioA®肛瘘栓总成功率分别为48/80(60%, 95%CI 48-71%)和1/4(25%, 95%CI 1-81%),疗效低于非CD肛瘘。5篇原创论文(13.6%)分析了复发率,术前采用免疫抑制剂治疗的患者成功率较低[61]。
至今还没有一项多中心、开放式、随机对照试验可重复这些理想结果。2016年Senejoux等对比研究了Surgisis®肛瘘栓与单纯挂线引流(对照组)治疗处于静止期或轻微活动期的106例CD患者,结果发现瘘管闭合和不良事件方面无差异[62]。
瘘管激光闭合术
这是一项新的保留括约肌手术,通过二极管激光摧毁瘘管上皮组织,进而消融整个瘘管。激光能量促使组织收缩和瘘管逐渐封闭。2011年Wilhelm发表了第一篇试验性研究,11例患者(非IBD患者)获得81.8%的瘘管一期愈合率,只有1例出现轻度不良事件[63]。Giamundo等在2015年回顾性报道纳入45例患者的单中心研究,2例PCD患者成功治愈[64]。
二氧化碳激光消融术在小样本、非对照、回顾性队列研究中也显现出良好结果[65]。
肛瘘癌变
据我们所知,还没有大样本、基于流行病学的研究来评估肛瘘相关性肛管癌(fistula-associated anal carcinoma, FAAC)的真正发病率。现有数据来自个案报道、回顾性队列研究和2010年的一项系统性回顾性分析,共收集61例患者[66,67]。FAAC被认为是一种少见病,发病率估计为0.004-0.7%[68]。它多发于病程长的瘘管患者,大部分病例病程超过15年。其确切发病机制尚不清楚,现有病因假说包括慢性炎症、长期应用免疫抑制、人乳头瘤病毒感染和吸烟[66,68,69]。腺癌,尤其是粘液腺癌,是目前最常见的组织学类型;鳞状上皮细胞癌也有报道[66]。因为FAAC是一种进展迅速的恶性肿瘤,且通常没有临床症状或临床症状不典型,所以大多数肿瘤被诊断时已处于进展期。长期存在肛周疾病的患者出现肛周或瘘管分增多,以及排便疼痛或其它恶化症状时都应引起怀疑,并采取MRI或EUA检查。一些作者提倡每年对病史超过10年的肛周疾病患者进行监测[69];然而,其他学者不推荐这种做法,因为FAAC发病率低,且缺乏有效的筛查方法[66,68]。
FAAC术后预后差,复发率高,尤其当直肠周围淋巴结受累时。辅助放化疗争议很多,应根据个体化原则应用;没有高级别证据支持放化疗作为常规疗法。此外,粘液腺癌被认为对放化疗无应答[69]。
结语
CPCD的诊治需要影像学医师、结直肠外科医师和消化科医生合作。诊断须包含详细的病史和体格检查,但还需辅助检查补充。MRI和EUS是主要的影像学评估方法。EUA仍是诊断与分型的金标准。EUA联合MRI或EUS可将准确度提高至100%。在开始使用免疫抑制剂治疗前,应用抗生素、手术引流或两者联合来控制脓肿是至关重要的。如果存在直肠炎,则必须治疗以提高其它治疗的效果。尽管缺少对照试验,但抗生素被推荐作为免疫抑制剂和手术治疗CPCD的辅助治疗。抗TNF制剂治疗CPCD拥有高级别证据,因此可以联合外科治疗作为一线治疗。
PCD领域未来发展的前景来自两个方向。我们正在获取新药治疗CD的数据,如果其中之一在PCD方面表现的特别活跃,这无疑将是一个重大福利。关于维多珠单抗和优特克单抗疗效的数据看起来不理想,但新的作用机制仍在持续探索中。另一个可能的方向是局部疗法的快速发展。在这个领域,干细胞治疗似乎是最具积极作用的疗法。其他推测的领域包括明确罹患PCD的遗传易感性基因、诊断技术的发展、以及关于长期疗效的治疗策略(相对于单一药物,例如在关键研究中探讨普遍性策略)。PCD患者承担着沉重的个人负担,且他们的疾病显著增加了医院就诊、药物治疗和手术的经济负担。因此,让我们真诚地希望未来几年带来治疗PCD的好消息。
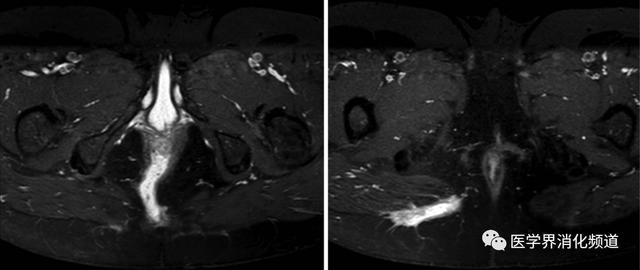
图1 经括约肌瘘。横截面,T1加权图像。(A)显示耻骨直肠肌下方高信号管道(长13cm)。(B)显示同一患者的瘘管延伸至臀大肌。

图2 复杂性肛周克罗恩病诊断流程。如果怀疑有肛周脓肿,MRI可以作为引流前的诊断方法[18]。
MRI, magnetic resonance imaging磁共振成像; EUS, endoanal ultrasound经肛腔内超声; EUA, examination under anesthesia麻醉状态下检查
|
表1 瘘管型克罗恩病的MRI、EUS、经会阴超声和EUA研究 | |||
|
作者和研究设计 |
组1 |
组2 |
结果 |
|
Siddiqui等[14]meta分析:4项随机试验(n=481) |
MRI |
EUS |
MRI:敏感度0.87(95%CI 0.63-0.96)、特异度0.69(95%CI 0.51-0.82) EUS:敏感度0.87(95%CI 0.70-0.95)、特异度0.43(95%CI 0.21-0.69) |
|
Maconi等[15]前瞻性、双盲对照研究(n=46) |
比较经会阴超声与EUS检查肛瘘和直肠阴道瘘的结果 |
无比较对象 |
经会阴超声:敏感度84.9% |
|
Schwartz等[16] 前瞻性、设盲对照研究(n=34) |
MRI、EUS和EUA |
准确率:MRI 87%(95%CI 69-96%),EUS 91%(95%CI 75-98%),EUA 91%(95%CI 75-98%) | |
|
Sahni等[17]系统性回顾:2项研究(n=156) |
MRI |
EUS |
MRI:敏感度0.97(95%CI 0.92-1.01)、特异度0.96(95%CI 0.91-1.02) EUS:敏感度0.92(95%CI 0.85-0.99)、特异度0.85(95%CI 0.75-0.95) |
|
MRI, magnetic resonance imaging磁共振成像; EUS, endoanal ultrasound经肛腔内超声; EUA, examination under anesthesia麻醉状态下检查; 95%CI, 95%confidence interval置信区间 | |||
|
表2 肛周疾病活动指数[19] | |
|
项目 |
分值 |
|
分泌物 | |
|
无分泌物 |
0 |
|
少量粘液性分泌物 |
1 |
|
中等量粘液性或脓性分泌物 |
2 |
|
大量分泌物 |
3 |
|
明显的粪便污染 |
4 |
|
疼痛/活动受限 | |
|
无活动受限 |
0 |
|
轻度不适,无受限 |
1 |
|
中度不适,部分受限 |
2 |
|
显著不适,显著受限 |
3 |
|
严重疼痛,严重受限 |
4 |
|
性生活受限 | |
|
无性生活受限 |
0 |
|
轻微受限 |
1 |
|
中度受限 |
2 |
|
显著受限 |
3 |
|
无法进行性生活 |
4 |
|
肛周疾病类型 | |
|
无肛周疾病 |
0 |
|
肛裂或粘膜撕裂 |
1 |
|
<3条肛瘘 |
2 |
|
>3条肛瘘 |
3 |
|
肛门括约肌溃疡或瘘管伴有显著皮损 |
4 |
|
硬结程度 | |
|
无硬结 |
0 |
|
小硬化 |
1 |
|
中等大小硬化 |
2 |
|
大硬结 |
3 |
|
显著波动感/脓肿 |
4 |
|
表3 瘘管型克罗恩病的抗生素试验 | |||
|
作者和研究设计 |
组1 |
组2 |
结果 |
|
Thia等[31]多中心、前瞻性、双盲、安慰剂对照研究(n=25) |
环丙沙星(500mg b.i.d)或甲硝唑(500mg b.i.d)治疗10周 |
安慰剂治疗10周 |
环丙沙星40%应答 vs. 甲硝唑14.3% vs. 安慰剂12.5%(P=0.43) |
|
Dejaco等[32]前瞻性、开放研究(n=52) |
环丙沙星(500-1000mg/d)和(或)甲硝唑(1000-1500mg/d)治疗8周 |
环丙沙星(500-1000mg/d)和(或)甲硝唑(1000-1500mg/d)治疗8周,从0或8周起加用硫唑嘌呤(2-2.5mg/kg) |
硫唑嘌呤组48%应答 vs. 无硫唑嘌呤组15%(P=0.03) |
|
West等[33]前瞻性、双盲、安慰剂对照研究(n=24) |
环丙沙星(1000mg/d)治疗12周,在6、8、12周加用英夫利息单抗5mg/kg |
安慰剂治疗12周, 在6、8、12周加用英夫利息单抗5mg/kg |
环丙沙星组73%应答 vs. 安慰剂组39%(P=0.12) |
|
Dewint等[34] 前瞻性、双盲、安慰剂对照研究(n=76) |
环丙沙星(500mg b.i.d)治疗12周,加阿达木单抗(160/80mg分别在0、2周,其它每周40mg)治疗24周 |
安慰剂治疗12周,加阿达木单抗(160/80mg分别在0、2周,其它每周40mg)治疗24周 |
环丙沙星组71%应答 vs. 安慰剂组47%(P=0.047) |
|
Maeda等[35] 前瞻性、双盲、安慰剂对照研究(n=74) |
10%甲硝唑软膏t.i.d治疗4周 |
安慰剂软膏治疗4周 |
甲硝唑组10/27 PCDAI评分至少降低5分 vs. 安慰剂组4/34(P=0.031) |
|
PCDAI, perianal Crohn’s disease activity index | |||
|
表4 瘘管型克罗恩病的免疫抑制剂试验、meta分析或系统性回顾分析 | |||
|
作者和研究设计 |
组1 |
组2 |
结果 |
|
Pearson等[36]meta分析:9项硫唑嘌呤或6-巯基嘌呤疗法的随机安慰剂对照研究 |
硫唑嘌呤或6-巯基嘌呤 |
安慰剂 |
硫唑嘌呤或6-巯基嘌呤治疗瘘管症状改善(风险比4.44; 95%CI 1.50-13.20) |
|
Sandborn等[37]多中心、前瞻性、双盲、安慰剂对照研究(n=48) |
口服他克莫司(0.2mg/kg/d)治疗10周 |
安慰剂治疗10周 |
他克莫司43%应答 vs. 安慰剂8%(P=0.004) |
|
Cat等[39]回顾性研究 |
第1周静脉注射环孢素(4mg/kg/d),随后口服环孢素(8mg/kg/d) |
无比较对象 |
80%患者在15和30天内症状改善,45%的瘘管在3、6、7、20个月时闭合 |
|
Yang等[41]系统性回顾分析:4项病例系列研究(n=40) |
沙利度胺(50-300mg/d) |
无比较对象 |
25%获得缓解,27.5%部分应答,35%因不良事件退出研究 |
|
95%CI,95%confidence interval置信区间 | |||
|
表5 瘘管型克罗恩病生物治疗试验 | |||
|
作者和研究设计 |
组1 |
组2 |
结果 |
|
Present等[42]多中心、前瞻性、双盲、安慰剂对照研究(n=94) |
在0、2、6周使用英夫利息单抗5mg/kg或10mg/kg |
安慰剂 |
所有瘘管完全闭合:5mg/kg剂量:55%,10mg/kg剂量:38%,安慰剂:13% |
|
Sands等[43] 多中心、前瞻性、双盲、安慰剂对照研究(n=195) |
每8周使用英夫利息单抗5mg/kg治疗54周 |
每8周使用安慰剂治疗54周 |
瘘管分泌物消失:英夫利息单抗组36% vs. 安慰剂组19%(P=0.009) |
|
Schwartz等[44]回顾性分析(n=21) |
环丙沙星(1000mg/d),硫唑嘌呤(2-2.5mg/kg/d)或6-巯基嘌呤(1-1.5mg/kg/d)及英夫利息单抗(5mg/kg在0、2、6周,以后每8周) |
无比较对象 |
瘘管分泌物消失:初期86%,远期76% |
|
Colombel等[48] 多中心、前瞻性、双盲、安慰剂对照研究(n=117) |
阿达木单抗(160/80mg在0/2周),然后每周40mg |
阿达木单抗(160/80mg在0/2周),然后使用安慰剂 |
瘘管分泌物消失:阿达木单抗组33%,安慰剂组13%(P=0.016) |
|
Schreiber等[49] 多中心、前瞻性、双盲、安慰剂对照研究(n=58) |
赛妥珠单抗(400mg每月) |
安慰剂 |
瘘管分泌物消失:赛妥珠单抗组36% vs. 安慰剂组17%(P=0.038) |
|
Sandborn等[50] 多中心、前瞻性、双盲、安慰剂对照研究(n=165) |
维多珠单抗(300mg)每4或8周 |
安慰剂 |
瘘管分泌物消失:维多珠单抗组41.2% vs. 安慰剂组11%(P=0.03) |
(本文仅供学术交流用途)
编辑及整理:夏璐
译者介绍
孙薛亮,医学硕士,苏州市中医医院肛肠科主治中医师。主持和参与苏州市科技局课题各1项,发表学术论文10余篇,获苏州市科技局新技术奖1项。
杨柏霖,男,医学博士。南京中医药大学附属医院结直肠外科主任医师、教授,硕士研究生导师。美国明尼苏达大学结直肠外科(2009年)和克利夫兰医学中心消化病研究所(2014年)访问学者。世界华人消化杂志编委,World Journal of Gastroenterology、Combinatorial Chemistry & High Throughput Screening审稿人。美国结直肠外科医师学会(ASCRS)会员,世界中医联合会盆底医学专业委员会常务理事,世界中医联合会肛肠病专业委员会理事,中国中西医结合大肠肛门病专业委员会委员,中国中西医结合大肠肛门病专业委员会IBD学组副组长,中国IBD联盟肛周疾病专业委员会副主任委员,中国医师协会外科分会肛肠学专业委员会委员。主持国家自然科学基金课题3项,发表SCI学术论文10余篇。
,







