分化型甲状腺癌(DTC)是最常见的甲状腺癌类型。据美国SEER数据库统计:甲状腺乳头状癌(PTC)占83.6%,甲状腺滤泡癌(FTC)占10.8%,甲状腺髓样癌(MTC)占2.2%,甲状腺未分化癌(ATC)占1.3%,其他类型如甲状腺低分化癌(PDTC)等占2.1%1。
手术、131I治疗与TSH抑制治疗是DTC的经典治疗手段,最终约10%~15%的患者会复发或进展成碘难治(RAIR-DTC),进而发展成局部晚期或全身晚期2;部分患者初诊时就已是晚期。虽然各大中心城市三甲医院专科的诊治水平和效果与美国相近;但由于基层规范化、同质化理论与技术培训的不足,我国甲状腺癌5年生存率与美国有约15%的差距3,4。近年来,随着靶向治疗为晚期患者带来了曙光,甲状腺癌的基因检测逐渐受到临床医生的关注。对甲状腺癌基因检测的研究进展与应用现状进行深入解读,诚邀广大读者共赏。
测序技术与甲状腺癌基因组学的研究进展
1.测序技术是肿瘤基因组学发展的核心推动力
2001年第一版人类基因组图谱的发布开启了基因检测序幕5。2006年人类肿瘤基因组图谱(TCGA)建立6,至今已积累33个癌种超过20,000例肿瘤患者的分子特征7,甲状腺癌基因图谱研究也获得快速发展8。
测序技术推动了肿瘤基因组学的进展6:第一代测序(sanger测序)准确性高,但成本高、通量低、不利于大规模应用9;第二代测序(NGS)成本低、通量高、自动化程度高,能够满足极短时间内对基因组进行高分辨率检测的要求9。目前在美国上市的三种商业化甲状腺癌基因检测平台均采用NGS目标靶向测序(Panel)技术10。基因检测技术的发展是推动肿瘤精准诊治的关键,也是各国争相攻占的核心技术制高点。
2.甲状腺癌基因组学研究进展
滤泡来源的甲状腺癌根据主要驱动突变可分为BRAFV600E样、RAS样两种类型11,12。前者主要包括BRAFV600E突变、RET融合基因,后者主要包括KRAS、NRAS、HRAS和BRAFV601E突变。甲状腺癌失分化或肿瘤进展的过程中,还可积累其他基因改变(Tp53突变、TERT突变、PI3K/PTEN/AKT通路突变等)11,12。BRAFV600E是PTC最常见的基因突变,在高侵袭性病理亚型中负荷更高11。TCGA研究中美国PTC人群BRAF突变检出率为59.7%8,中国PTC人群检出率高达72.4%13。
尽管仍处于临床初期应用或研究阶段,甲状腺癌的临床和病理表观与基因的关系已逐渐引起临床医生的高度重视。
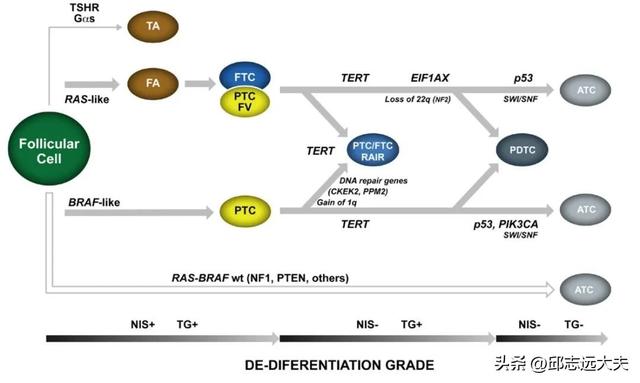
图:甲状腺肿瘤演进过程中的基因改变14
甲状腺癌基因检测的循证依据
1.指南推荐近年来,欧美及中国权威甲状腺癌指南对基因检测适应症、检测标志物组套的推荐和推荐强度大同小异(表)。学会, 发表时间基因检测的适应症检测标志物推荐强度ATA, 201515推荐15A:细胞学无法确诊的甲状腺结节(AUS/FLUS)患者BRAF, NRAS, HRAS, KRAS, RET/PTC1, RET/PTC3, PAX8/PPARγ等弱推荐推荐16A:细胞学检查为滤泡性肿瘤(FN)或可疑滤泡性肿瘤(SFN)的患者BRAF, RAS, RET/PTC, PAX8/PPARγ等弱推荐推荐17A:细胞学检查为可疑乳头状癌(SUSP)的患者BRAF突变或7个基因突变组套(BRAF, RAS, RET/PTC, PAX8/PPARγ)弱推荐推荐52:目前不推荐使用分子检测来指导术后放射性碘治疗的使用-不推荐ESMO, 201916应为所有MTC患者提供遗传咨询和筛查生殖系RET突变RET突变强推荐无法切除或有远处转移的ATC患者,应检测BRAFV600EBRAFV600E突变中等程度推荐CSCO, 2021 17术前FNA检查结果为AUS/FLUS或FN/SFN的患者特定基因突变(如BRAFV600E, RET/PTC, RAS, PAX8/PPARγ等)、多基因检测或单一基因突变II级推荐手术标本的分子检测BRAF、RAS、TERT启动子突变等II级推荐NCCN, 202218推荐THYR‐1:术前FNA检查结果为AUS/FLUS或FN/SFN,但无提示恶性的临床特征和/或影像学征象2A类推荐推荐PAP‐9、FOLL‐8和HÜRT‐8:残存肿瘤/局部复发或远处转移的、不适合RAI治疗的DTC患者,出现了晚期、进展性或威胁生命的病变可治疗的基因突变(ALK, NTRK, RET基因融合)、DNA错配修复缺陷(dMMR)、微卫星不稳定性(MSI)和肿瘤突变负荷(TMB)推荐MEDU‐1:疑诊甲状腺髓样癌推荐MEDU‐2:甲状腺髓样癌手术后筛查胚系RET原癌基因突变(10,11,13–16号外显子)推荐MEDU‐6:残存肿瘤/局部复发的甲状腺髓样癌,起始RET抑制剂或帕博利珠单抗治疗前RET突变和肿瘤突变负荷(TMB)推荐ANAP‐1:疑诊甲状腺未分化癌推荐ANAP‐3:计划积极治疗的IVC期(远处转移)甲状腺未分化癌可治疗的基因突变(BRAF, NTRK, ALK, RET, MSI, dMMR和肿瘤突变负荷)表: 国内外甲状腺癌指南对基因检测的推荐注:ATA=美国甲状腺学会,ESMO=欧洲肿瘤学会,CSCO=中国临床肿瘤学会,NCCN=美国国立综合癌症网络,AUS=意义不明确的细胞非典型病变,FLUS=意义不明确的滤泡性病变,FNA=细针穿刺活检2.不同时机基因检测的意义不同病理类型的甲状腺癌,基因检测的目的、结果判读、处理方式有所不同。针对DTC,基因检测主要用于术前辅助良恶性鉴别、手术方案参考,以及手术后131I治疗方案参考、判断预后和指导晚期肿瘤的靶向治疗。针对MTC,基因检测主要用于遗传病(瘤)定性、手术方案参考、辅助判断预后、指导晚期肿瘤的靶向治疗等。辅助术前诊断:目前术前细针穿刺细胞学标本的基因诊断证据,主要来自Bethesda分类为III类和IV类甲状腺结节的良恶性鉴别。最终临床处理方案应综合临床表现、超声特点和基因诊断结果进行制定17。辅助判断DTC预后:BRAFV600E突变降低甲状腺癌细胞钠/碘同向转运体(NIS)表达,增加进展至RAIR-DTC的风险19。PTC患者若合并BRAFV600E突变,复发20及死亡21风险分别增加2.2倍、1.66倍。多种基因突变联合是近年研究热点,例如BRAFV600E联合TERT突变,病灶更容易丧失摄碘能力22,23且复发风险更高24。指导靶向药物治疗:靶向治疗是RAIR-DTC和晚期甲状腺的重要治疗方式。多靶点酪氨酸激酶抑制剂可延长无进展生存期,但提高总生存期方面仍有争议,并且此类药物靶标较宽,发挥疗效的同时很可能伴随药物的相关不良反应,减低患者生活质量。而在进行靶向特定基因突变/融合的单靶点抑制剂(如选择性RET抑制剂、NTRK抑制剂)治疗前,需进行基因检测筛选靶点,指导药物的选择18。基因检测在甲状腺癌临床管理中应用的现状与反思1.临床实践中基因检测存在的问题基因检测技术应用过快,但其检测结果成熟度与稳定性还远不到临床可靠判断的水准,主要原因有以下几个方面。疾病层面:基础研究对癌发生的完整基因通路并没有完全揭秘,一些问题尚无答案25。例如:部分PTC个例并未发现已知基因突变,驱动基因是什么?诱发和维持甲状腺癌的细胞信号网络全貌是怎样的?人才层面:解读报告结果能力水平落后。调查显示,大于30%以上肿瘤科医生每月NGS检测量超过5个,而中国超过90%以上临床医生需要NGS报告解读支持26。以BRAFV600E突变解读为例,并非所有BRAFV600E突变都意味着复发高危,低危、中危、高危的患者均可存在BRAFV600E突变15。技术层面:现有基因检测技术的特异性、稳定性、结果判定标准和质量控制并没有达到其他常规检验项目的临床实践水平,证据水平仅为辅助或参考。监管层面:公司品牌、检测技术(测序仪、试剂耗材、测序靶集、测序场地及流程等)、成本与资源的控制还在市场竞争或完善监管的路上27。2.对基因检测现状的反思基因(分子)诊断从起点至今,发展成分子病理学及临床精准医学模式仅经历了20余年,但对传统医学模式的冲击与改变已经十分明显。既往,我们一直从临床表现去寻找疾病的特征与证据来看其内因,从表观现象来判断诊治结果;或通过分析临床大数据来寻找外表的规律,从而建立起各种临床诊疗的规范(如教科书或指南)。时至今日,精准医学模式将从个体、细胞、分子水平寻找表观事件的本因,力图从内因解读开始揭示疾病或健康的秘密,也许这才是未来临床医学、预防医学的发展方向。在临床实践中,我们首先看到目前绝大多数临床医生对基因检测的目的、适应证和临床意义并不清楚或专业;而现有的检测报告解读模式导向均以靶向药物的选择为主,故既不能满足临床专业人士的需求且有误导作用;加之现今基因检测技术与质量控制体系尚未完善或统一,所以检测技术应用超前与解读结果水平严重落后的矛盾十分突出。很显然,现有的临床基因检测方式或报告解读模式与实践需求差距甚远,我们需要更为“精准”地解读报告。
总结
甲状腺癌与基因改变的“因果关系”尚未完全阐明。目前临床除少数晚期甲状腺癌的基因检测是为了明确是否有治疗靶点外,更多的基因检测是为了预测生物学行为。相对于传统的病理诊断,基因(分子)检测对临床治疗决策与预后的价值远不明确,仅为“辅助或参考”级别证据。临床工作中应持续强调:重视病理诊断与分型信息的准确性,对基因检测报告结果既不能不信,亦不能全信。所以,提高基因检测报告的专业解读水平、控制基因检测的过度使用、开展分子诊断辅助病理准确分型的研究势在必行。
,




