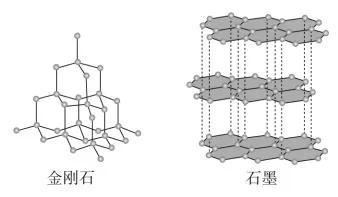
一、分子动理论
1、物质是由大量分子组成的
(1)单分子油膜法测量分子直径
(2)1mol 任何物质含有的微粒数相同 N = 6.02*1023 /mol
(3)对微观量的估算
①分子的两种模型:球形和立方体(固体液体通常看成球形,空气分子占据的空间看成立方体)
②利用阿伏伽德罗常数联系宏观量与微观量

2、分子永不停息的做无规则的热运动(布朗运动 扩散现象)
(1)扩散现象:不同物质能够彼此进入对方的现象,说明了物质分子在不停地运动,同时还说明分子间有间隙,温度越高扩散越快
(2)布朗运动:它是悬浮在液体中的固体微粒的无规则运动,是在显微镜下观察到的。
①布朗运动的三个主要特点:永不停息地无规则运动;颗粒越小,布朗运动越明显;温度越高, 布朗运动越明显。
②产生布朗运动的原因:它是由于液体分子无规则运动对固体微小颗粒各个方向撞击的不均匀性造成的。
③布朗运动间接地反映了液体分子的无规则运动,布朗运动、扩散现象都有力地说明物体内大量的分子都在永不停息地做无规则运动。
(3)热运动:分子的无规则运动与温度有关,简称热运动,温度越高,运动越剧烈。
3、分子间的相互作用力
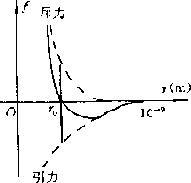
分子之间的引力和斥力都随分子间距离增大而减小。但斥力随分子间距离加大而减小得更快,如图虚线所示。
分子间同时存在引力和斥力,两种力的合力又叫做分子力。图象中实线表示引力和斥力的合力(即分子力)随距离变化的情况。
当两个分子间距在图象横坐标 r0 距离时,分子间的引力与斥力平衡,分子间作用力为零, r 的数量级为10-10 m,r 0位置叫做平衡位置。当分子距离的数量级大于10r0 时,分子间的作用力变得十分微弱,可忽略不计。
4、温度
宏观上的温度表示物体的冷热程度,微观上的温度是物体大量分子热运动平均动能的标志。热力学温度与摄氏温度的关系: T = t 273.15K
5、内能
①分子势能
分子间存在着相互作用力,因此分子间具有由它们的相对位置决定的势能,这就是分子势能。
分子势能的大小与分子间距离有关,分子势能的大小变化可通过宏观量体积来反映。当 r >r0 时,分子力为引力,当r 减少时,分子力做负功,分子势能较少。当 r <r0 时,分子力为斥力,当r 减少时,分子力做负功,分子势能增加。因此 r =r0 时分子势能最小。
②物体的内能
物体中所有分子热运动的动能和分子势能的总和,叫做物体的内能。
一切物体都是由不停地做无规则热运动并且相互作用着的分子组成,因此任何物体都是有内能的。(理想气体没有分子势能只有分子动能,理想气体内能只取决于温度)
③改变内能的方式:做功与热传递。
二、气体
6、气体实验定律
①一定质量气体等温变化:玻意耳定律PV = C (C 为常量)
适用条件:压强不太大,温度不太低。
微观解释:一定质量的理想气体,温度保持不变时,分子的平均动能是一定的,在这种情况下,体积减少时,分子的密集程度增大,气体的压强就增大。
图象表达: P=c/V

②一定质量的气体等容变化:查理定律P/T= C (C 为常量)
适用条件:温度不太低,压强不太大。
微观解释:一定质量的气体,体积保持不变时,分子的密集程度保持不变,在这种情况下,温度升高时,分子的平均动能增大,气体的压强就增大。
图象表达: P-V

③一定质量的气体等压变化:盖吕萨克定律: V/T=C (C 为常量)
适用条件:压强不太大,温度不太低。
微观解释:一定质量的气体,温度升高时,分子的平均动能增大,只有气体的体积同时增大,使分子的密集程度减少,才能保持压强不变。
图象表达:V-T
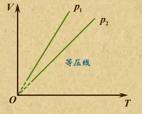
7、理想气体
定义:任何情况下都严格遵守三个实验定律的气体。它是一种理想模型,实际并不存在。
(在常温常压下,大部分气体都可以看成理想气体。)
微观上:分子间的作用力可以忽略不计,故一定质量的理想气体的内能只与温度有关,与体积无关。
理想气体的状态方程:PV/T=C
8、气体压强的微观解释
大量气体分子频繁的撞击容器壁,产生持续的压力。
影响气体压强的因素:①气体的平均分子动能(温度)
②分子的密集程度即单位体积内的分子数(体积)
三:物态和物态变化
9、晶体:外观上有规则的几何外形,有确定的熔点,一些物理性质表现为各向异性。
非晶体:外观没有规则的几何外形,无确定的熔点,一些物理性质表现为各向同性。
①判断物质是晶体还是非晶体的主要依据是有无固定的熔点。
②晶体与非晶体并不是绝对的,有些晶体在一定的条件下可以转化为非晶体(例如:晶体石英可转化为非晶体玻璃)。
10、单晶体和多晶体
如果一个物体就是一个完整的晶体,如食盐小颗粒,这样的晶体就是单晶体(单晶硅、单晶锗)。
如果整个物体是由许多杂乱无章的小晶体排列而成,这样的物体叫做多晶体。多晶体没有规则的几何外形,但同单晶体一样,仍有确定的熔点。
11、表面张力
当表面层的分子比液体内部稀疏时,分子间距比内部大,表面层的分子表现为引力。如露珠。
12、液晶
分子排列有序,各向异性,可自由移动,位置无序,具有流动性。
各向异性:分子的排列从某个方向上看液晶分子排列是整齐的,从另一方向看去则是杂乱无章的。
四:热力学定律
13、改变系统内能的两种方式:做功和热传递
①热传递有三种不同的方式:热传导、热对流和热辐射。
②这两种方式改变系统的内能是等效的。
③区别:做功是系统内能和其他形式能之间发生转化;热传递是不同物体(或物体的不同部分)之间内能的转移。
14、热力学第一定律
①表达式u2-u1 = W Q
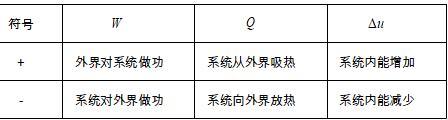
15、能量守恒定律
能量既不会凭空产生,也不会凭空消失,它只能从一种形式转化为另一种形式,或者从一个物体转移到另一物体,在转化和转移的过程中其总量不变。
第一类永动机不可制成,因其违背了热力学第一定律。
第二类永动机不可制成,因其违背了热力学第二定律(一切自然过程总是沿着分子热运动的无序性增大的方向进行)
熵是分子热运动无序程度的定量量度,在绝热过程或孤立系统中,熵是增加的。
16、能量耗散
系统的内能流散到周围的环境中,没有办法把这些内能收集起来加以利用。