[核心素养发展目标] 1.了解科学施用化肥、合理用药的重要性,不科学施用的危害,增强使用化学品的“科学态度与社会责任”。2.通过合理使用化肥、农药及合理用药的学习,了解常见化学品的分类及成分,培养“科学探究与创新意识”。
一、化肥、农药的合理施用

1.合理施用化肥
(1)合理施用化肥的重要性:保证农作物增产,减少农作物损失。
(2)合理施用化肥考虑因素
①土壤酸碱性,作物营养状况。
②化肥本身性质,如硝酸铵受热或经撞击易爆炸,应改性处理后施用。
(3)不合理施用化肥危害
①过量施用不仅浪费,也可能导致水体富营养化,如水华等污染现象。
②影响土壤酸碱性和土壤结构。
2.合理施用农药
(1)农药类别

(2)农药不合理施用的危害
①破坏生态平衡,使一些害虫产生抗药性
②使对农药敏感的有益昆虫大量死亡
③使土壤、作物的农药残留超标,造成环境污染
④造成大气、地表水和地下水污染
(3)长期使用滴滴涕(DDT)的危害
①使害虫对DDT产生抗药性

(1)大雨天追肥有利于农作物的吸收( × )
提示 大雨天追肥会造成化肥随雨水流失,浪费且污染环境。
(2)硝铵(NH4NO3)可直接作化肥使用( × )
提示 NH4NO3在受热或撞击时会发生爆炸。
(3)豆科植物在生长过程中不需要经常施用铵态化肥( √ )
提示 豆科植物可以将空气中的氮气转化为化合态的氮,故不需经常施用氮肥。
(4)化肥、农药可以促进农作物的生长,提高农作物产量,因此可大量施用( × )
提示 不合理施用化肥、农药会导致环境污染,作物残留超标等危害。
(5)既然农药、化肥的施用有危害,因而就不施用( × )
提示 农药、化肥的施用对农业生产有着重要意义,要合理施用。
(6)石灰硫黄合剂是一种植物杀菌剂,是合成农药( × )
提示 石灰硫黄合剂是无机农药,不属于合成农药。

1.在农业生产中是否应该继续施用化肥和农药的小组辩论中,正方小明和反方小刚分别叙述了自己的观点:
(1)下面事实不能支持小明观点的是________(填字母,下同)。
A.可以解决快速增长的人口吃饭问题
B.可以促进农作物生长,杀灭害虫,形成良性的生态循环
C.合成农药用量少、见效快
D.降低了农业生产成本,可以促进农业机械化、规模化发展
答案 B
(2)持反方观点的小刚从生态系统、害虫的抗药性及食品中化肥、农药的残留等方面进行了驳斥,下列两例事实是小刚对滥用杀虫剂造成的恶性循环的论证:事实1.在远离施药地的南极,在海鸟和鱼体都检测出了某些农药成分。事实2.喜马拉雅山的积雪中也发现了某些农药成分。这些事实说明________。
A.农药、化肥被考察队或登山者带到南极或高山上
B.农药、化肥的滥用已影响到全球的生态循环
C.农药、化肥成分可以在生态链中富集,导致生物链系统发生变化
答案 BC
2.瑞士化学家米勒因合成DDT于1948年获得诺贝尔医学奖,DDT的合成为人类的卫生防疫事业做出了巨大贡献,但研究表明,DDT是一种难降解的有毒化合物,进入人体内会引起慢性中毒,我国1983年停止生产和使用。
写出DDT(

1.硫酸铵是农村常用的一种铵态氮肥,田间一次施用过多会使植物变得枯萎发黄,俗称“烧苗”,其原因是( )
A.植物从土壤中吸收的养分过多
B.植物根细胞不能从土壤中吸水
C.植物的根系不能将养分向上运输了
D.根系的呼吸作用加剧、释放的能量过多了
答案 B
解析 当施用化肥过多时,根细胞不能从土壤中吸水而发黄。
2.下列现象,不是化肥的不合理施用导致的是( )
A.乡村农田周围的小河河水发绿发臭,鱼虾大面积死亡
B.长期耕垦的农田出现土壤酸化,土壤板结
C.长期耕种的农田重金属元素、有毒物质超标
D.城市的空气中PM2.5含量超标,雨水酸度增强
答案 D
解析 城市空气PM2.5含量超标、雨水酸度增强和汽车尾气、工业废气排放有关。
3.“六六六”是一种有机杀虫剂,高效、低毒、杀虫活性宽广,其结构简式为

,下列说法正确的是( )
A.属于烃类化合物
B.分子式为C6H6Cl6
C.该化合物易溶于水
D.该化合物对光、空气等表现不稳定,容易降解
答案 B
解析 该化合物分子中含C、H、Cl三种元素,分子式为C6H6Cl6,属于氯代物,不为烃,故B正确,A错误;“六六六”难溶于水,对光、空气、酸碱表现出很稳定的化学性质,难于降解,故C、D错误。
4.拟除虫菊酯是一类高效低毒,对昆虫具有强烈触杀作用的杀虫剂。其中对光稳定的溴氰菊酯的结构简式如下:
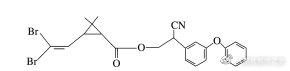
下列对该化合物叙述正确的是( )
A.在一定条件下可以和H2发生加成反应
B.该化合物含有4种官能团
C.该化合物在酸性条件下稳定
D.该化合物含有苯环,属于芳香烃
答案 A

1.药物的分类

2.药物在人体内作用方式
(1)改变机体细胞周围的物理及化学环境。
(2)药物分子和机体生物大分子的功能基团相结合。
3.常见药物阿司匹林的制备、功能及不适症状
(1)制备

(2)功能及不适症状
功能:解热镇痛
不适症状:长期大量服用可能会导致胃痛、头痛、眩晕、恶心等症状
4.合理用药遵循原则及因素
(1)原则:安全、有效、经济、适当等原则
(2)

5.滥用药物危害
(1)滥用安眠药或镇静剂、抗生素、兴奋剂对个人机体产生严重的影响。
(2)吸食毒品对个人和社会带来极大危害。

(1)生活中食用的药物大多是天然药物( × )
提示 大多是合成药物。
(2)小苏打片可以治疗胃病,主要是可以中和过多的胃酸,缓解胃部不适( √ )
(3)药物属于商品,患者可以在药店随意购买( × )
提示 处方药需要凭医生处方才能获得,非处方药(OTC)可以自行购买。
(4)安眠药可以帮助睡眠,因此每当失眠时就可以服用安眠药( × )
提示 安眠药为处方药,必须在医生的指导下服用,不能滥用。
(5)青少年年龄还小,偶尔吸食一点毒品危害不大,教育教育就好( × )
提示 吸毒对个人和社会造成极大危害,青少年一定要远离毒品。

1.胃舒平是常见家用胃药,说明书如图:

根据以上说明书内容,回答以下问题。
(1)服用胃舒平时嚼服比吞服效果好的原因是什么?写出Al(OH)3和胃酸作用的化学方程式。
提示 服用胃舒平治疗胃酸过多的反应原理是氢氧化铝和盐酸反应生成氯化铝和水。反应物间的接触面积越大,反应越充分且反应速率越快,因此嚼服可以增大药物和胃酸的接触面积,便于充分反应,和胃酸(主要为盐酸)反应的方程式为:Al(OH)3+3HCl===AlCl3+3H2O。
(2)医生建议胃舒平连续服用不可以超过7天,为什么?
提示 长期服用可导致严重便秘,有可能导致肠梗阻,老年人长期服用会引起骨质疏松,肾功能不全者易引起铝中毒。
(3)怎么设计实验证明胃舒平药片中含有氢氧化铝?写出相关的离子反应方程式?
提示 可以利用Al(OH)3的两性来验证
方案1:取3片胃舒平药片碾碎,置于试管中,加入足量的稀盐酸,充分反应,过滤,取滤液,向滤液中加入稀氢氧化钠溶液至过量
现象:向滤液中加入稀氢氧化钠溶液,先生成白色沉淀,后沉淀又部分溶解
相关离子方程式:Al(OH)3+3H+===Al3++3H2O
MgCO3+2H+===Mg2++CO2↑+H2O
H++OH-===H2O,Al3++3OH-===Al(OH)3↓
Mg2++2OH-===Mg(OH)2↓
Al(OH)3+OH-===AlO2(-)+2H2O
方案2:取3片胃舒平药片碾碎,置于试管中,加入适量的氢氧化钠溶液,过滤,取滤液,向滤液中加入稀盐酸至过量
现象:向滤液中加入稀盐酸,先生成白色沉淀,后沉淀完全溶解
相关离子方程式:Al(OH)3+OH-===AlO2(-)+2H2O
H++OH-===H2O
H++AlO2(-)+H2O===Al(OH)3↓
Al(OH)3+3H+===Al3++3H2O
2.2019年6月26日是国际禁毒日,宣传主题为“珍爱生命,拒绝毒品”。毒品的危害,可概括为“毁灭自己,祸及家庭,危害社会”12个字,结合毒品及其危害,回答以下问题。
(1)下列药物,属于毒品的有________(填字母,下同)。
a.海洛因 b.甲基苯丙胺(冰毒)
c.吗啡 d.三聚氰胺
e.阿司匹林 f.大麻
(2)下列有关青少年和毒品关系的说法,错误的是______。
A.青少年吸食毒品会严重危害其身心健康
B.青少年好奇心强,偶尔吸食一点,很快就会提神,学习效率高
C.青少年吸食毒品,会造成家庭巨大的经济和精神损失
D.青少年年龄还小,吸食毒品不会危害社会
E.个别青少年思想空虚,吸食毒品寻求刺激,最终可能会导致严重的个人、家庭和社会问题
(3)如图是毒品大麻的结构简式:

,下列有关大麻性质的说法错误的是________。
A.大麻分子中含两种官能团
B.大麻能使酸性KMnO4溶液褪色
C.1 mol 大麻可以和足量单质钠反应生成2 mol 氢气
D.1 mol大麻可以在一定条件下和7 mol H2发生加成反应
答案 (1)abcf (2)BD (3)C
解析 毒品的危害很大,青少年吸食毒品,很容易成瘾,危害个人、家庭及社会,青少年一定要远离毒品。据大麻的分子结构,大麻分子中含—OH和

两种官能团,可以使酸性KMnO4溶液褪色,1 mol大麻和足量钠反应,可生成1 mol氢气,苯环和碳碳双键都可以和H2在一定条件下加成,需要7 mol氢气。

1.合理用药应当包括的要素是( )
A.科学性、有效性、安全性、经济性和适当性
B.安全性、有效性、规律性、经济性、适当性
C.科学性、舒适性、规律性、经济性、可口性
D.舒适性、长效性、新颖性、安全性、规律性
答案 A
解析 合理用药,必须在医生、药师的指导下,遵循科学性、有效性、经济性、安全性和适当性进行用药。
2.阿司匹林是一种常用的解热镇痛药物,其结构简式为

,关于阿司匹林的性质的合理使用,以下说法错误的是( )
A.阿司匹林可以和NaHCO3反应生成CO2
B.1 mol阿司匹林和NaOH反应,最多需要1 mol NaOH
C.阿司匹林应避光,密闭于干燥处保存,如果受潮,服用后会强烈地刺激胃
D.阿司匹林应当饭后吃,主要为了避免阿司匹林在胃中溶解,而强烈刺激胃
答案 B
解析 阿司匹林分子中含有羧基,可以和NaHCO3反应生成CO2,A正确;该分子可以在碱性条件下水解,生成物再和NaOH反应,1 mol最多需要3 mol NaOH,B错误;阿司匹林水解会生成强刺激性的水杨酸和乙酸,会强烈地刺激胃,故C、D正确。
3.摇头丸是神经麻醉性毒品,吸食摇头丸对人体的呼吸系统、心血管系统及肝肾脏均会产生严重影响,其结构简式为:

,下列关于摇头丸的描述,错误的是( )
A.摇头丸有麻醉神经的作用,长期服用,可能导致神经病
B.摇头丸分子中含有羟基,能和Na反应生成氢气
C.摇头丸毒性很强,吸食后容易上瘾,年轻人不要尝试
D.摇头丸可以和乙酸在一定条件下发生中和反应
答案 D
解析 根据摇头丸的结构特点,分子中含有羟基,可以和钠反应放出氢气,也可以和乙酸发生酯化反应,故D错误。
课时对点练A组 基础对点练
题组一 化肥的施用及对环境的影响
1.尿素是人工合成的有机物,其结构简式为

,下列关于尿素的叙述不正确的是( )
A.尿素是一种氮肥
B.尿素是人体新陈代谢的一种产物
C.尿素在水中可以电离出NH4(+)
D.尿素的分子式为CH4N2O,是一种有机氮肥
答案 C
解析 据尿素的结构简式,尿素分子中不含NH4(+),在溶液中也不能电离出NH4(+)。
2.欲同时对农作物施用含N、P、K三种元素的化肥,现有:①K2CO3;②KCl;③Ca(H2PO4)2;④(NH4)2SO4;⑤氨水。最适合的组合是( )
A.①②③ B.②③④
C.①③⑤ D.②③⑤
答案 B
3.下面有关化肥与环境关系的描述,正确的是( )
A.雨天追肥有利于农作物的吸收
B.大量施用化肥对环境没有污染
C.绿色植物都能直接在空气中进行生物固氮
D.过多的尿素进入水体会恶化水质,导致“水华”现象
答案 D
解析 雨天追肥,化肥易随雨水流失;大量施用化肥,会造成土壤、水的污染;固氮是把游离态的氮转化为化合态的氮,有些植物如豆科植物,可直接在空气中进行固氮,而其他大部分植物不行;尿素进入水体会导致水体富营养化,最终使水体恶化,形成“水华”现象。
题组二 农药的合理使用与环境污染
4.制取漂白粉、配制波尔多液和石灰硫黄合剂及改良酸性土壤时,都要用到的物质是( )
A.硫黄 B.熟石灰
C.胆矾 D.石膏
答案 B
解析 漂白粉是由Cl2与Ca(OH)2反应制得;波尔多液是CuSO4与石灰。
5.六氯苯是被联合国有关公约禁止或限制使用的有毒物质之一。下式中能表示六氯苯的是( )

答案 B
6.为了避免或减少污染环境,科学家研制出多种新型杀虫剂,以代替DDT,如图的化合物就是其中的一种。下列关于该化合物说法不正确的是( )

A.该化合物不属于芳香烃
B.在一定条件下,可以发生加成反应
C.在一定条件下,可以发生酯化反应
D.该化合物能溶于水
答案 D
解析 结构中不含有苯环,且含有氧原子,故不属于芳香烃,A项正确;由于含碳碳双键和醛基,故可加成,B项正确;由于含羟基,所以可以发生酯化反应,C项正确;该有机化合物不溶于水,故D项错误。
题组三 合理用药与人体健康
7.下列对用药的说法正确的是( )
A.根据自己需要,就可以在药店购买抗菌药物
B.“是药三分毒”,所以任何药品都有可能引起不良反应
C.处方药用药后出现不良反应,说明医生处方有问题
D.药品使用说明中列举的不良反应越少的药越好
答案 B
解析 合理用药必须在医生、药师的指导下,遵循安全、有效、经济和适当的原则,处方药不能在药店随意购买,任何药都会出现不良反应,无论是处方药还是非处方药,故A、C、D错误,B项正确。
8.所谓合理用药是( )
A.配药准确
B.价格低廉
C.对症开药
D.以药物和疾病为基础,安全、有效、经济、适当地用药
答案 D
9.每年的6月26日是“世界禁毒日”。下列有关毒品的叙述,错误的是( )
A.吸毒会影响人的神经系统、循环系统和呼吸系统的生理功能
B.吸毒能感受到强烈的快感或兴奋,可以少量使用
C.吸毒极易成瘾,严重危害人体身心健康、危害社会
D.毒品用量过度会引起吸食者猝死
答案 Bhttps://www.renjiaoshe.com/jiaocai/2055.html
解析 毒品危害个人、家庭和社会,极易成瘾,不能食用,故B错误。
10.丙烯可用于合成杀除根瘤线虫的农药(分子式为C3H5Br2Cl)和应用广泛的DAP树脂:

已知
①R—Cl+H2ONaOHR—OH+HCl
②酯与醇可发生如下酯交换反应:
RCOOR′+R″OH催化剂△RCOOR″+R′OH(R、R′、R″代表烃基)
(1)农药C3H5Br2Cl分子中每个碳原子上均连有卤原子。
①A的结构简式是______________,A含有的官能团名称是________________;
②由丙烯生成A的反应类型是______________。
(2)A水解可得到D,该水解反应的化学方程式是___________________。
(3)C蒸气密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为:碳60%,氢8%,氧32%。C的结构简式是_____________。
答案 (1)①CH2==CHCH2Cl 氯原子、碳碳双键 ②取代反应
(2)CH2==CHCH2Cl+H2ONaOHCH2==CHCH2OH+HCl
(3)CH3COOCH2CH==CH2
解析 (1)由农药(C3H5Br2Cl)分子中每个碳原子上均连有卤原子,推出丙烯→A发生的是取代反应,A为

。(3)结合C的相对密度和各元素的质量分数推出其化学式为C5H8O2,由框图可得C的结构简式为CH3COOCH2CH==CH2。
B组 综合强化练
1.过多的植物营养物质如尿素[CO(NH2)2]等进入水体会恶化水质,导致“水华”现象。尿素属于( )
A.磷肥 B.氮肥
C.钾肥 D.复合肥料
答案 B
2.随着生活水平的提高,人们越来越重视“绿色食品”,绿色食品是指( )
A.添加了绿色色素的食品
B.含有叶绿素的食品
C.原料生产过程中没有使用化肥、农药的食品
D.原料生产及加工过程中没有受到污染的食品
答案 D
解析 绿色食品是指在生产、加工各个环节都没有受到污染的食品。它以“环保、安全、健康”为目标,在农作物生长过程中严格控制,不使用对人体有害的农药、化肥、生长调节剂等。
3.NH3是一种重要的化工原料,可以制备一系列物质(如图)。下列说法正确的是( )

A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.NH3和NO2在一定条件下可以发生氧化还原反应
D.图中所涉及的盐类物质均可发生水解
答案 C
解析 本题通过氨气作为化工原料制取多种产品的分析,考查含氮化合物的性质和转化关系。NH4Cl是常用的化肥,而NaHCO3不是化肥,A项错误;NH4Cl、HNO3受热时都易分解,而Na2CO3受热不易分解,B项错误;根据氮元素化合价分析,氮元素可以发生化合价归中的氧化还原反应,C正确。
4.农业上用的杀菌剂波尔多液由硫酸铜和石灰乳按一定比例配制而成,它能防治植物病毒的原因是( )
A.硫酸铜使菌体蛋白质盐析
B.石灰乳使菌体蛋白质水解
C.菌体蛋白质溶解于波尔多液
D.铜离子和石灰乳使菌体蛋白质变性
答案 D
解析 铜盐属于重金属盐,石灰乳呈强碱性均能使蛋白质变性。
5.敌敌畏是一种对人畜都有毒性的杀虫剂,其结构简式为:

,施用后能迅速分解,无残留,植物收获前7天禁用,下列对敌敌畏的说法不正确的是( )
A.敌敌畏在酸性及碱性条件下都不稳定
B.敌敌畏对人畜都有毒害,吃了刚打过敌敌畏农药的水果有中毒的风险
C.敌敌畏能和H2发生加成反应
D.敌敌畏不能使酸性KMnO4溶液褪色
答案 D
解析 根据敌敌畏的结构,分子中含有

,故能使酸性KMnO4溶液褪色,故D项错误。
6.达菲是一种治疗甲型和乙型流感的药物,工业上可用莽草酸合成达菲,两者结构简式如下,下列有关莽草酸和达菲的说法不正确的是( )

莽草酸 达菲
A.莽草酸的分子式为C7H6O5
B.莽草酸和达菲都能使溴水褪色
C.莽草酸和达菲都能发生加成反应和取代反应
D.莽草酸和达菲在溶液中都能电离出H+
答案 A
解析 据莽草酸的结构简式,可确定其分子式为C7H10O5,故A错误;据两者的结构简式,两者分子中都含
,故都能使溴水褪色,B、C项正确;莽草酸中含有—COOH,达菲分子中含有H3PO4,故都能电离出H+,D正确。
7.请你参与识别化肥的探究活动。有五种化肥分别是硫酸钾、氯化钾、碳酸氢铵、氯化铵和硝酸铵。
第一步:称取五种化肥各10 g,分别研细。
第二步:硝酸铵和熟石灰反应的化学方程式是_________________________。
第三步:另取三种铵盐各少量,分别盛于三支试管中,均滴入少量盐酸,无明显现象的是____________,有气泡放出的是________,反应的化学方程式是__________________。
第四步:另取氯化铵和硝酸铵两种铵盐进行识别,写出识别时发生反应的化学方程式:_____________________。
第五步:取两种钾盐,分别在试管中配成溶液,各滴入几滴氯化钡溶液,生成白色沉淀的钾盐是________,无明显现象的钾盐是________。
答案 2NH4NO3+Ca(OH)2===Ca(NO3)2+2NH3↑+2H2O 氯化铵和硝酸铵 碳酸氢铵 NH4HCO3+HCl===NH4Cl+CO2↑+H2O NH4Cl+AgNO3===NH4NO3+AgCl↓ K2SO4 KCl
解析 三种铵盐首先滴加盐酸,有气体产生的是碳酸氢铵,另外两种铵盐无明显现象;氯化铵和硝酸铵的鉴别可用滴加AgNO3溶液来区分,有白色沉淀生成的是氯化铵,硝酸铵无明显现象。涉及的反应有2NH4NO3+Ca(OH)2===Ca(NO3)2+2NH3↑+2H2O、NH4HCO3+HCl===NH4Cl+CO2↑+H2O、NH4Cl+AgNO3===NH4NO3+AgCl↓、K2SO4+BaCl2===BaSO4↓+2KCl。
8.瑞士化学家米勒因合成DDT于1948年获得诺贝尔医学奖。在第二次世界大战中的1944年,美国在意大利的许多士兵因使用DDT来扑灭传染斑疹伤寒流行病人身上的虱子而避免丧生。联合国世界卫生组织曾评价说:“单独从疟疾病者,DDT可能拯救了5 000万生命。”但进一步的观察和研究表明,DDT是一种难降解的有毒化合物,进入人体内可引起慢性中毒。我国已于1983年停止生产和使用。
(1)杀虫剂“1605”本身对人畜毒性远强于DDT,但DDT已被禁用,而“1605”尚未禁用,这是因为________________________________________________________________________
________________________________________________________________________。
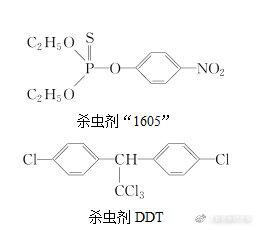
杀虫剂DDT
由结构分析知:“1605”在使用过程中,不能与_____________________________________
物质混合使用,否则会因________________________________________________________。
(2)DDT可以用电石(CaC2)为原料经以下途径而制得:
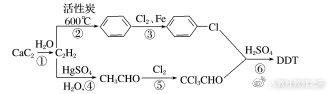
写出④⑤⑥步反应的化学方程式:
④________________________________________________________________________,
⑤________________________________________________________________________,
⑥________________________________________________________________________。
答案 (1)“1605”在降解酶作用下易从P—O处降解为毒性小、不残存的物质(20天可消失一半),而DDT不易降解,它长期滞留于动物体或食物链内,危害性大(其他合理答案也可) 碱性 水解而失效






