古语有云:酒壮怂人胆,说的是人会在酒精的作用下,做很多平时不敢做的事。酒精或者说乙醇为什么会有这么大的魅力呢?乙醇又具有怎样的结构和性质?开始我们今天的学习吧。(本文系化学biu一biu原创首发,转载请联系授权)
今天的知识要点有:1 乙醇的结构 2烃的衍生物和官能团的概念 3 乙醇的性质 4.乙醇的用途和安全问题
本套讲义知识点讲解较为全面,适合查缺补漏和自学,需要必修二全套知识讲义的也可以私信小天老师,打印出来,学习效果更佳~最后通过几个题目巩固加深本讲知识点,一定要做完再看解析哦,如果有不清楚的地方,欢迎与小天老师交流。

要点一、乙醇的结构
乙醇的分子结构可以看成是乙烷分子(CH3CH3)中的氢原子被-OH取代的产物,也可以看成是水分子(H—OH)中的氢原子被乙基(—CH2CH3)取代后的产物。其分子式为C2H6O,结构式为


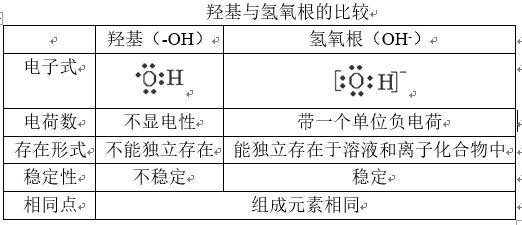
结构简式为CH3CH2OH或C2H5OH。乙醇分子中含有-OH原子团,这个原子团叫羟基,它决定着乙醇的化学性质。
要点二、烃的衍生物和官能团的概念
1、烃的衍生物
从结构上说,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。从组成上看:烃的衍生物除含碳、氢元素外,还含有氧、卤素、氮、硫等元素中的一种或几种。如初中化学里学过的甲醇(CH3OH)、乙醇(CH3CH2OH)及前面学过的一氯甲烷(CH3Cl)、硝基苯(C6H5NO2)、溴苯(C6H5Br)等都属于烃的衍生物。
2、官能团
在烃的衍生物中,其中取代氢原子的其他原子或原子团使烃的衍生物具有不同于相应烃的特殊性质,这种决定有机物的化学特性的原子或原子团叫做官能团。如卤素(-X)、羟基(-OH)、硝基(-NO2)等都是官能团,再如决定烯烃性质的“C=C”,所以“C=C”是烯烃的官能团。
要点三、乙醇的性质
1、乙醇的物理性质
乙醇俗称酒精,是无色透明、有特殊香味、易挥发的液体,密度比水小,沸点为78.5℃,能与水以任意比互溶,可溶解多种无机物和有机物,是良好的有机溶剂。
要点诠释:
①通过生活中酒类的浓度可以证明乙醇能与水以任意比互溶。

②由工业酒精制无水酒精的方法:先在工业酒精中加入生石灰,然后加热蒸馏制得无水酒精。
③通常用无水CuSO4(白色)检验是否含有水。
2、乙醇的化学性质
(1)乙醇与钠的反应
反应方程式:2C2H5OH 2Na→2C2H5ONa H2↑
实验现象:金属钠沉于无水乙醇底部,在钠表面有无色气泡产生,最终钠粒消失,溶液为无色透明。收集产生的气体,移近酒精灯火焰,有爆鸣声。
反应原理:该反应中,金属钠置换了羟基上的氢(即断氧氢键),说明-OH上的氢原子比较活泼。

要点诠释:
a.钠的密度(0.97g/cm3)小于水而大于乙醇,所以钠浮于水面而沉于乙醇底部。
b.钠与乙醇反应不如钠与水反应剧烈,说明乙醇羟基中的H不如水中的H活泼,乙醇比水更难电离,所以醇无酸性,是非电解质。
c.产物C2H5ONa遇水会强烈水解,生成强碱NaOH。
d.该反应为置换反应。
e.乙醇与活泼金属(K、Mg、Al、Ca等)也能发生类似反应,置换出氢气,如:2C2H5OH Mg→(C2H5O)2Mg H2↑。
f.实验室中,常用乙醇销毁散落的钠的小颗粒,不用水。

(2)乙醇的氧化反应
①乙醇的燃烧
乙醇在空气里能够燃烧,发出淡蓝色的火焰,产生大量的热。

②乙醇的催化氧化

实验现象:灼烧至红热的铜丝离开火焰时变为黑色,插入无水乙醇中后又变为红色。几次实验重复之后,试管内的液体有刺激性气味。



要点四、乙醇的用途和安全问题
乙醇的用途:作燃料、有机溶剂、消毒剂(医用75%的酒精)、酿酒、化工原料等。
酒也给我们带来了不少危害,很多不法分子利用酒精的溶解性制造假酒;由于饮酒造成的交通事故屡见不鲜。化学带给我们的不仅仅是利或弊,关键是正确看待,科学合理利用。

典型例题




这些题目觉得如何?如果化学学习上有遇到任何问题欢迎与小天老师联系哦~
,




