
2021年10月发表在Haematologica上的一篇文章,简略介绍了治疗多发性骨髓瘤(MM)三种最新的免疫疗法:抗体药物偶联物(ADC)、双特异性抗体或 T 细胞结合抗体(TCE)和嵌合抗原受体细胞 (CAR-T),以及目前正处于不同阶段——已批准上市、正在Ⅰ、Ⅱ期临床试验的新药,阐述了新药的结构特点,并对这些新药的疗效和面临的问题进行了概括总结。小编带大家了解一下。
背景
新型免疫治疗方法被认为是多发性骨髓瘤(MM)的新一代治疗手段。在这个快速发展的领域中,全面概述新型免疫疗法具有很多的挑战。本文章将重点介绍三种最先进的新型免疫疗法:靶向以下抗原的抗体药物偶联物(ADC)、双特异性抗体或T细胞结合抗体(TCE)和嵌合抗原受体细胞(CAR-T)。
抗原
信号淋巴细胞激活分子家族成员7 (SLAMF7)
SLAMF7(或CS1)在各种淋巴细胞上表达, 包括B和T细胞, 自然杀伤细胞和浆细胞的亚群。SLAMF7是单克隆抗体埃罗妥珠单抗的靶点。针对SLAMF7研发CAR-T细胞可能更具挑战性,因为这种抗原在T细胞亚群上的表达可能导致自相残杀。
分化簇 38 (CD38)
在浆细胞上表达的CD38,是达雷妥尤单抗和isatuximab等单克隆抗体的靶点。
B细胞成熟抗原 (BCMA)
BCMA优先表达于成熟的B细胞,包括浆细胞。它对B细胞的发育很重要,对增殖和生存也很关键。BCMA是肿瘤坏死因子受体(TNFR)超家族中的一员,一种细胞表面受体,与B细胞激活因子 (BAFF) 和增殖诱导配体 (APRIL) 结合。
跨膜激活剂及钙调亲环素配体相互作用分子(TACI)
TACI 是另一个在 B 细胞亚群和浆细胞上表达的肿瘤坏死因子受体超家族成员。
分化簇19 (CD19)
CD19 广泛表达在 B 细胞上, 却较少表达在浆细胞上。据推测, 它可能在“骨髓瘤干细胞”上表达。最近通过超分辨率显微镜的分析发现, CD19更广泛但低水平表达在一部分骨髓瘤细胞 (10%-80%) 上。
G蛋白偶联受体C5家族亚型D (GPRC5D)
GPRC5D 是一种孤儿受体, 在正常和恶性浆细胞上普遍表达, 但在除毛囊免疫豁免组织外的一般组织上不表达。
Fc受体同系物5 (FcRh5)
FcRH5, 又称FcRL5、IRTA2和CD307, 是一个120 kDa的蛋白, 与经典的Fc受体具有序列同源性。FcRH5在MM细胞和浆细胞上表达, 在正常B细胞上表达较少。
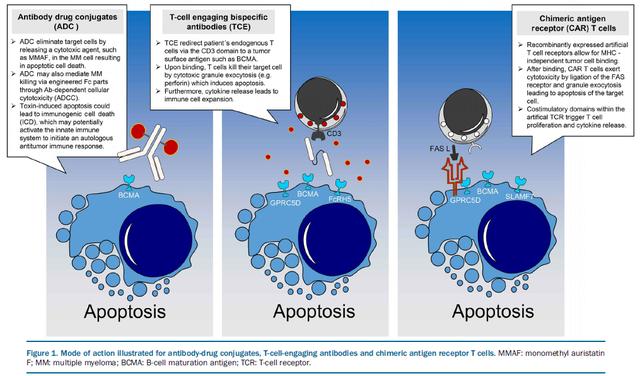
抗体药物偶联物
ADC是细胞毒性小分子药物通过生物活性连接子 (Linker) 与单克隆抗体偶联, 在与骨髓瘤细胞上相应的靶蛋白结合后, ADC被骨髓瘤细胞内吞, 细胞毒性药物在骨髓瘤细胞内释放;它们可以被认为是靶向化疗药物。不同的ADC有不同的靶蛋白、连接子或细胞毒性效应分子 (payload) 。
Belantamab mafodotin
迄今为止, 临床上最先进的 ADC 是 Belantamab mafodotin, 这是一种抗 BCMA的人源化 IgG1 单克隆抗体, 通过非裂解Linker与微管破坏剂单甲基 auristatin-F (MMAF) 偶联。 MMAF 在 G2/M 期阻滞骨髓瘤细胞周期, 诱导细胞凋亡。 ADC 的Fc 区被无岩藻糖基化, 增强了对天然免疫细胞 Fc 受体的亲和力, 从而增强了免疫介导的识别和消除。 因此, Belantamab mafodotin也可以被认为是免疫疗法。Belantamab mafodotin 的 MMAF 成分导致临床上显著的眼毒性:角膜的微囊样上皮改变。角膜病变是最常见的不良事件, 导致剂量减少和延迟, 以及永久停止治疗。因此, 用这种新型ADC治疗MM患者时, 必须定期做眼科检查。DREAMM-2 研究表明 Belantamab mafodotin 作为单药具有显著的临床疗效, 并于 2020 年在美国和欧洲获得批准 (剂量为每 3 周 2.5 mg/kg) 用于治疗四线治疗后 (包括蛋白酶体抑制剂、免疫调节剂和抗CD38单抗) 的RRMM患者。
MEDI2228
MEDI2228是另一种靶向BCMA的ADC。细胞毒性部分是tesirine, 一种可与DNA 结合的吡咯并苯并二氮杂 (PBD) 二聚体, 通过可被蛋白酶裂解的Linker, 偶联到抗体上。这种毒素诱导 DNA 链间交联和 DNA 损伤反应。该ADC被设计成专门针对膜结合的BCMA蛋白, 因此其活性不受可溶性BCMA水平的影响。
AMG 224
ADC AMG 224 是一种靶向BCMA的IgG1 单克隆抗体, 与微管蛋白抑制剂 mertansine (也称为 DM1) 偶联。
CC99712
目前正在Ⅰ期研究 (NCT04036461) 中评估的 ADC CC99712 也是靶向 BCMA。 它的毒性载荷是微管蛋白抑制剂单甲基auristatin E。
TAK-169 和 TAK-573
TAK-169 和 TAK-573 是两种处于早期临床开发阶段的靶向CD38的ADC。TAK-169 与去免疫化志贺毒素 A 亚基相连。临床前研究证明, TAK-169在体外高效裂解原代 MM 细胞。目前尚无关于正在进行的Ⅰ期研究 (NCT04017130) 的临床数据。
TAK-573 靶向 CD38的 表位预计不会与目前已批准的抗 CD38 单克隆抗体达雷妥尤单抗 (Daratumumab) 和isatuximab发生交叉反应。它与两个减毒干扰素 α2b 分子相连。一项人类首次、剂量递增的Ⅰ期试验 (NCT 3215030) 也在评估不同的治疗方案, 目前正在招募患者。早期药代动力学和免疫学参数的数据显示, 在所有四个治疗组中MM患者的临床反应有限。
FOR-46
MMAF偶联的ADC FOR-46, 目前正在进行I期剂量递增研究 (NCT03650491) , 针对补体调节蛋白CD46。这种ADC以CD46的肿瘤特异性抗原识别表位为靶点, 有效地诱导巨噬细胞。
HDP-101
ADC HDP-101的细胞毒性作用是基于一种合成的含绿盖鹅膏的鹅膏菌毒素, 一种RNA聚合酶Ⅱ特异性抑制剂。这种对基因转录和蛋白质合成的抑制与细胞周期无关, 这是一个重要的特性, 因为在许多情况下 大部分 MM 细胞不增殖。这种罕见的特性可能是HDP-101在临床上的一个重要特征。由于其在染色体的位置, RNA聚合酶II经常与TP53在del(17p)中共同缺失。因此, 具有这种高风险特征的MM细胞可能对HDP-101高度敏感。有前景的临床前安全性和药物活性研究数据已被报道, 对RRMM患者进行首次人体I期剂量递增和扩增研究计划于2021年开展。

双特异性抗体
双特异性 TCE 代表了另一种治疗 MM 的方法, 它利用了 T 细胞高效的细胞溶解活性。一方面与浆细胞或 B 细胞谱系相关抗原结合, 另一方面通过 CD3 结构域募集 T 细胞, 从而使 T 细胞靠近 MM 细胞, 最终导致颗粒酶和穿孔素分泌以及靶细胞凋亡。
AMG 420
最近一项关于BCMA的双特异性T细胞衔接蛋白(BiTE®) AMG 420的研究为这种策略的有效性提供了原理证明。与CD19xCD3 BiTE®贝林妥欧单抗 (Blinatumomab) 一样, AMG 420的半衰期较短, 从循环中迅速消除。因此有必要在数周内连续输液, 给患者带来极大的不便。鉴于其他多个半衰期更长的TCE新型药物正在进行临床研究, 生产厂家没有继续开发AMG 420。在2020年的ASH年会上提交了许多关于TCE的摘要, 并报告了至少7种新TCE的初步临床数据。
Teclistamab
Teclistamab(JNJ-64007957) 是一种人源化双特异性 IgG4 抗体, 可与靶细胞上的 BCMA 和 T 细胞上的 CD3 (BCMA x CD3) 结合。 目前正在I 期研究中进行评估, Teclistamab 有静脉注射和皮下注射两种制剂, 每周给药一次。 由于随访时间有限 (中位随访时间为3.9个月) , 这些反应是否持久, 以及高度浆细胞增殖性疾病或髓外病变的患者是否有类似的获益, 仍有待观察。一项II期研究已经启动。
REGN5458
REGN5458是另一种结合BCMA和CD3的TCE, 在一项剂量递增的I期研究中对45例患者进行了评估。REGN5458每周静脉注射一次, 然后进入维持阶段, 每2周注射一次。REGN5458的第二阶段研究目前正在招募患者。
TNB383B
TNB383B是一种BCMA x CD3的完全人源性IgG4抗体, 改善了与细胞表面BCMA的结合, 半衰期为2-3周, 每 3 周给药一次, 静脉注射给药。对CD3的亲和力下降可能是TNB383B 的细胞因子释放综合征 (CRS) 发生率较低的原因。
AMG 701
AMG 701是AMG 420的衍生物, 具有改良的BiTE®结构, 半衰期延长至112小时左右, 适合每周一次给药。
PF-06863135
PF-06863135 是一种 BCMA x CD3 人源化 IgG2a 抗体, 正在进行的一项 I 期研究对PF-06863135的皮下制剂进行评估。
CC-93269
这种不对称、双臂、基于人源化IgG 的BCMA x CD3抗体也正在进行I期研究评估。BCMA在浆细胞上的特异性和一致性表达使其成为T细胞免疫治疗的理想靶蛋白。然而, 其他一些细胞表面受体也具有这些特征, 并且正在进行的试验中以TCE为目标。这一点特别值得关注, 因为有报道称, 在使用靶向免疫疗法治疗后, BCMA下调, 甚至BCMA表达不可逆缺失。
Talquetamab
Talquetamab是一种 GPRC5D x CD3 TCE, 已在一项剂量递增的I期研究中进行了评估, 研究通过静脉注射和皮下注射给药。
Cevostamab
这种基于 FcRH5 x CD3 人源化 IgG 的 TCE 正在 I 期剂量递增和扩增试验 (NCT03275103) 中进行评估。FcRH5 在 MM 细胞和浆细胞上表达, 在正常B细胞上表达较少。

嵌合抗原受体T细胞疗法
CAR T 细胞已成为一种极具前景的癌症治疗新方法。以CD19为靶点的CAR T细胞在B细胞恶性肿瘤如侵袭性淋巴瘤和急性淋巴细胞白血病中首次获得成功。主要的毒性反应是CRS、免疫效应细胞相关的神经毒性综合征 (ICANS) 和血细胞减少症, 这些毒性反应可能会持续一段时间。最近在开发用于治疗 MM 的 CAR T 细胞方面取得了进展。CAR T细胞通过未受刺激的白细胞采集T细胞, 并通过慢病毒或逆转录病毒融合CAR基因获得, 该结构带有识别肿瘤抗原的抗体片段和T细胞受体信号域CD3ζ, 以激活修饰的T细胞 (第一代) 。为了进一步加强T细胞的激活, 加入一个 (第二代) 或两个 ( 第三代 ) 共刺激结构域, 通常来自CD28或4-1BB。在体外扩增后, CAR T 细胞在用环磷酰胺和氟达拉滨进行淋巴细胞清除化疗后重新输注, 以增强修饰的 T 细胞的扩增。在骨髓瘤细胞上已经确定了几个潜在的目标, 其中BCMA的数据最为成熟。美国国立卫生研究院采用BCMA-CD28 CAR进行了首次人体试验。
Idecabtagene vicleucel
已有关于 idecabtagene viceucel (ide-cel, bb2121) 和 ciltacabtagene autoleucel 最新的数据报告。
Ciltacabtagene autoleucel
Ciltacabtagene autoleucel (cilta-cel, LCAR-B38M或JNJ-4528) 是一种具有两个BCMA结合域的BCMA-4-1BB构建体, 首先在中国开发。
同种异体嵌合抗原受体T细胞
目前可用的自体CAR T细胞疗法的缺点包括:在目前的临床试验中, 由于患者经过大量预处理, 产生CAR - T细胞所需的时间长, T细胞的活性下降。这一点可以通过在病程早期预先收集T细胞来部分克服。现成的异体CAR T细胞可能是一种选择。
Mailankody等人在2020年的ASH会议上展示了首个用于RRMM的同种异体BCMA CAR -T细胞研究的初步数据。在这些异体CAR T细胞中, T细胞受体被敲除以避免移植物抗宿主疾病, CD52被敲除以允许使用抗CD52抗体进行选择性和长时间的淋巴细胞清除以改善移植。基因编辑是用转录激活因子样效应物核酸酶 (TALEN) 技术进行的。CAR转化的自然杀伤性脐带血细胞可能是另一个未来现成的细胞产品的潜在来源。

讨论
随着大量的新型免疫治疗方法和治疗策略目前处于临床开发的所有阶段, 包括一些监管机构最近批准的方法和策略, MM的治疗格局可能在未来5年迅速发展, 就像大约30年前引入大剂量治疗和自体造血干细胞移植, 或本世纪头十年蛋白酶体抑制剂和免疫调节剂的发展, 以及近年来单克隆抗体的出现, 都是如此。这些新型药物显示出前所未有的单药活性, RRMM患者ORR超过80%, 缓解时间也超过1年, 即使在没有其他治疗选择的患者中也是如此。然而, 目前还没有III期临床数据集。因此, 在日常临床实践中, 何时以及如何使用这些免疫治疗药物仍有许多悬而未决的问题。
参考文献:
1. Leo Rasche, Ralph Wäsch, Markus Munder, et al. Novel immunotherapies in multiple myeloma – chances and challenges. Haematologica. 2021 Oct 1;106(10):2555-2565.
,




