撰文:CCL
编辑:CCL

相关基础理论
在多相催化循环中,吸附、迁移、反应、脱附,每一步都涉及化学键的断裂与形成。而键的断裂、生成与催化剂和反应物质的电子特性息息相关。结合大量实验现象与理论计算模型,人们已经确证电子结构在多相催化中的核心作用。在具有表面有机配体的纳米催化剂中,表面配体会导致纳米颗粒表面电子结构的变化,从而影响催化反应活性和选择性。电子结构变化的程度取决于表面配体与催化剂的相互作用强度。
具体而言,这一相互作用产生于表面有机分子的分立分子轨道和金属表面离域的电子态之间,可以分为两个方面:1.电荷转移,2.极化作用。作用的结果是导致金属纳米颗粒费米能级的移动和表面化学势的变化,如下图1所示:
图 1

2、改变不同反应物和产物在催化剂表面的吸附能
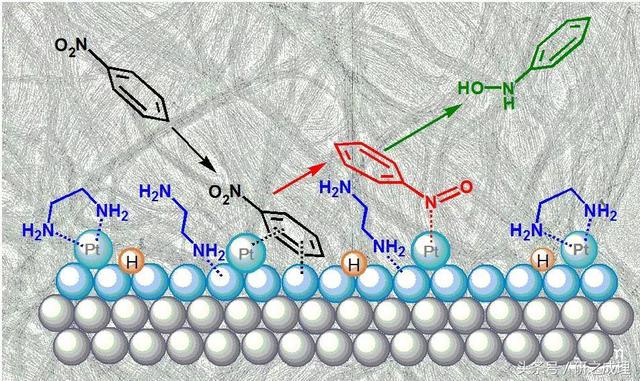
多相催化反应过程中,吸脱附过程是非常重要的一个环节。有机配体的电子效应有可能改变催化剂表面对不同物质的吸附能力,从而影响催化反应的活性和选择性。例如在2016年的这篇Nature materials中(ref.2, 如下3图),文中主要考察Pt纳米线催化剂表面电子效应对硝基苯选还原反应活性和选择性的影响。研究发现Pt纳米线催化剂在乙二胺的影响下,其表面变为富电子结构,从而对欠电子的底物,比如:硝基苯,的吸附能力增强,而对富电子苯羟胺的吸附能力减弱,最终实现硝基苯选择性还原成为苯羟胺。
图 3
12年Nano letter(ref 3, 下图4)报道随着Pt纳米颗粒表面胺配体负载量的增加,催化剂表面对不同底物的吸附能力也发生不同程度的变化。文中以4-辛炔的加氢还原作为模型反应。理论计算结果表明当有机配体胺的含量达到一定程度,催化剂对不同底物的吸附能力排序如下:4-辛炔 > 有机配体 > 4-辛烯。正是这一吸附能力的变化,导致目标产物辛烯的产量显著增加。
图 4

3、对催化反应过程中活化熵的影响
表面配体对催化反应的影响通常会理解为反应活化能的改变。需要注意的是,表面配体的引入,无论是电子效应还是空间体积效应,可能对催化反应过程的活化熵产生影响,最终改变反应的活性或者选择性。比如在2010的这篇nature material中(ref 4),作者发现当Pd/Al2O3负载型催化剂表面修饰不同链长的烷基硫醇配体后,环氧丁烯(EpB)加氢的选择性显著增加,并且链长越长,反应活性越高(见下图5)。文中将链长与反应活性的关系归结为反应过程中的熵障碍。链长越短、熵障碍越大。
图 5

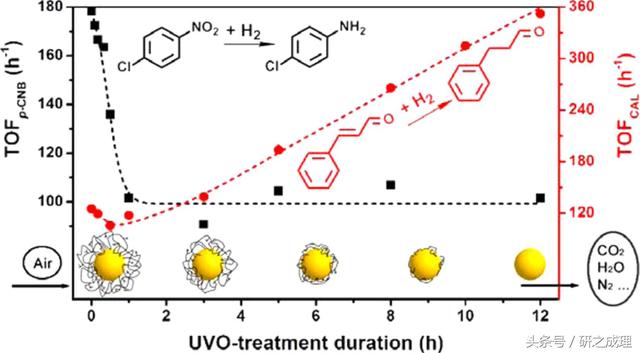
同样在2014年的这篇ACS Catalysis(ref 5)中,作者发现当Au-PVP/SiO2(其中,Au为纳米颗粒,PVP为配体,SiO2为载体)表面配体被祛除后,其对对氯硝基苯(p-CNB)加氢反应的催化活性显著降低,见下图6。文中将这一反应活性降低归结为活化熵的改变。没有有机配体存在,p-CNB在催化剂表面活动性受限,见下图6。熵显著减低,从而降低反应活性。
图 6
总而言之,对于多相纳米催化中表面配体的电子效应,需要注意的有以下几点:a. 电子效应的来源:有机配体d轨道与金属表面电子态之间的耦合作用,从而产生电荷转移或者极化作用。两者比较而言,电子转移作用的影响程度远大于极化作用。b.电子效应究竟如何影响催化反应活性和选择性?:可以简单分为三类:1.引导新活性物种的产生;2.改变催化剂表面对不同底物的吸附能力;3.对反应活化熵的影响。当然,电子效应不总是产生正面促进催化的效果,也很有可能产生负面抑制作用。
表面配体对催化反应的影响可以分为电子效应和空间体积效应两大部分。对于本文中提到的大部分参考文献,我们后期都会进行深入解读,敬请期待。
声明:本文主要内容来自于综述 “Untangling the Role of the Capping Agent in Nanocatalysis: Recent Advances and Perspectives”,Catalysts 2016, 6, 185;
参考文献:
1.Effect of electronic structures of clusters stabilized by poly(N-vinyl-2-pyrrolidone) on aerobic oxidation catalysis. J. Am. Chem. Soc. 2009, 131, 7086 – 7093.
2.Interfacial electronic effects control the reaction selectivity of platinum catalysts. Nat. Mater. 2016, 15, 564–569.
3. Capping ligands as selectivity switchers in hydrogenation reactions. Nano Lett. 2012, 12, 5382–5388.
4. Controlled selectivity for palladium catalysts using self - assembled monolayers. Nat. Mater. 2010, 9, 853–858.
5. Impacts of organic stabilizers on catalysis of Au nanoparticles from colloidal preparation. ACS Catal. 2014, 4, 3982–3993.
,